题目内容
11.向含有AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,若有气泡产生,则滤出的固体一定为( )| A. | Ag、Cu两种单质的混合物 | B. | Cu、Fe两种单质的混合物 | ||
| C. | Ag、Fe两种单质的混合物 | D. | Ag、Cu和Fe三种单质的混合物 |
分析 根据金属活动性顺序可知,铁>铜>银.向含有AgNO3、Cu(NO3)2的废液中加入一定量的铁粉,铁粉会首先置换硝酸银中的银,待硝酸银完全反应后继续与硝酸铜发生反应;过滤,向滤渣中滴加稀硫酸,有气泡产生,说明滤渣金属中含有铁,即加入的铁粉过量.据此分析.
解答 解:因为向滤渣中滴加稀硫酸,有气泡产生,说明滤渣中有铁粉,即所加的铁粉过量,那说明原混合溶液中的银和铜全部被置换出来,即滤液中肯定没有AgNO3、Cu(NO3)2,则滤出的固体中一定含有Ag、Cu、Fe;
故选项为:D.
点评 本题是对金属活动性顺序的考查,解题的关键是掌握金属活动性顺序表的意义,只有这样才能做出正确的判断.

练习册系列答案
相关题目
10.用100mL量筒进行相关实验,操作正确的是( )
| A. |  量取20.2mL水 | B. | 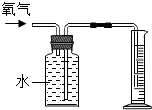 收集80mL氧气 | ||
| C. | 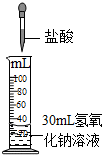 向30mL氢氧化钠溶液中滴入盐酸 | D. |  配制100g10%的氯化钾溶液 |
19.现有25g久置的生石灰,测得其中钙元素与碳元素的质量比为10:1,在室温下,将该化合物与100g稀盐酸混合,恰好完全反应,所得的不饱和溶液的质量为120.6g,则原化混合物中钙元素的质量为( )
| A. | 10g | B. | 12g | C. | 14g | D. | 16g |
1.能与稀盐酸发生中和反应的是( )
| A. | 生石灰 | B. | 石灰石 | C. | KOH溶液 | D. | 锌粒 |
 宏观--微观--符号之间建立联系是化学学科特有的思维方式.汽车尾气是造成大气污染的主要原因之一,在汽车排气管上安装“催化转化器”便可以将汽车的尾气转化成无毒气体.如果用
宏观--微观--符号之间建立联系是化学学科特有的思维方式.汽车尾气是造成大气污染的主要原因之一,在汽车排气管上安装“催化转化器”便可以将汽车的尾气转化成无毒气体.如果用 表示碳原子,用
表示碳原子,用 表示氧原子,用
表示氧原子,用 表示氮原子,图为气体转换的微观过程,请你根据图示回答下列问题.
表示氮原子,图为气体转换的微观过程,请你根据图示回答下列问题.
