题目内容
15.在标准状况下,体积为8.96L的CO和CO2的混合气体共14.4g.(1)CO的质量为5.6g.
(2)CO的体积为4.48L.
(3)混合气体的平均摩尔质量为36g•mol-1.
(4)混合气体的密度为1.6g•L-1.
分析 在标准状况下,1mol任何气体的体积都是22.4L;
物质的量=$\frac{物质的质量}{物质的摩尔质量}$.
解答 解:混合气体物质的量为:=$\frac{8.96L}{22.4L•mol-1}$=0.4 mol,
设混合气体中CO物质的量为x,则CO2的物质的量为:0.4mol-x,
根据题意有:2836g•mol-1×x+4436g•mol-1×(0.4mol-x)=14.4g,
x=0.2mol,
则二氧化碳物质的量为:0.4mol-0.2mol=0.2mol,
(1)一氧化碳的质量为:0.2 mol×28g•mol-1=5.6g,
(2)一氧化碳的体积为:0.2 mol×22.4L•mol-1=4.48L,
(3)混合气体的平均摩尔质量为:$\frac{14.4g}{0.4mol}$=36g•mol-1,
(4)混合气体的密度为:$\frac{14.4g}{8.96L}$=1.6g•L-1.
故填:5.6;4.48;36;1.6.
点评 本题主要考查物质的量、摩尔质量、摩尔体积多方面的转化关系,要注意掌握.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
5.点燃下列混合气体,不会发生爆炸的是( )
| A. | 氢气和氮气 | B. | 氢气和空气 | C. | 一氧化碳和氧气 | D. | 甲烷和空气 |
6.用铝箔包裹着2.3g金属钠投入到足量水中,理论上可以收集到氢气的物质的量为( )
| A. | 0.05mol | B. | 0.2mol | ||
| C. | 大于0.05mol小于或等于0.2mol | D. | 无法判断 |
3.推理是一种重要的学习和研究方法.下列推理正确的是( )
| A. | 单质中只含一种元素,所以只含一种元素的物质一定是单质 | |
| B. | 化学变化前后物质的质量总和不变,所以1gH2和1gO2一定能够生成2gH2O | |
| C. | 碱性溶液能使酚酞溶液变红,所以能使酚酞溶液变红的物质一定呈碱性 | |
| D. | 中和反应有盐和水生成,所以有盐和水生的反应一定是中和反应 |
7.将一定量的双氧水和3克的二氧化锰混合,充分反应,测得反应的总质量(m)与反应肘间(t)的数据如下表所示:
根据题目要求,问双氧水的物质的量是多少?(通过化学方程式列式计算)
| 反应时间t/s | t0 | t1 | t2 | t3 | t4 | t5 |
| 总质量m/g | 50 | 49.0 | 48.1 | 47.3 | 46.8 | 46.8 |
4.元素周期表是化学学习和科学研究的重要工具,下列对于元素周期表的使用方法不正确的是( )
| A. | 查阅元素在自然界中的分布 | |
| B. | 确定元素的种类 | |
| C. | 查阅某种元素的相对原子质量 | |
| D. | 利用原子序数,在元素周期表中查找该元素的元素符号及元素名称 |
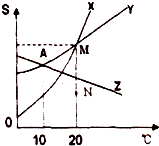 图是X、Y、Z三种物质的溶解度曲线,
图是X、Y、Z三种物质的溶解度曲线,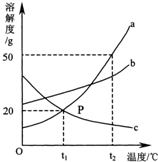 如图是a、b、c三种固体物质的溶解度曲线图,请回答:
如图是a、b、c三种固体物质的溶解度曲线图,请回答: