题目内容
完成下列反应的化学方程式,并回答有关问题.
(1)铁丝在氧气中燃烧 ,属于 基本反应类型;
(2)一氧化碳在空气中燃烧: ,该反应是 反应(选填“吸热”或“放热”);
(3)碳酸氢铵加热分解: ,化肥“碳铵”应该 保存;
(4)曾青得铁则化为铜: ,铁的表面出现 色固体;
(5)铁片放在稀硫酸中反应 ,反应后溶液颜色呈 色.
(1)铁丝在氧气中燃烧
(2)一氧化碳在空气中燃烧:
(3)碳酸氢铵加热分解:
(4)曾青得铁则化为铜:
(5)铁片放在稀硫酸中反应
考点:书写化学方程式、文字表达式、电离方程式,物质发生化学变化时的能量变化,反应类型的判定
专题:化学用语和质量守恒定律
分析:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答:解:(1)铁在氧气中燃烧生成四氧化三铁,反应的化学方程式为3Fe+2O2
Fe3O4;该反应符合“多变一”的特征,属于化合反应.
(2)一氧化碳在空气中燃烧生成二氧化碳,反应的化学方程式为:2CO+O2
2CO2;该反应属于放热反应.
(3)碳酸氢铵易分解产生氨气、水和二氧化碳,反应的化学方程式为NH4HCO3
NH3↑+CO2↑+H2O;碳酸氢铵受热以分解,化肥“碳铵”应该阴凉处密封保存.
(4)“曾青得铁则化为铜”说的是将铁放入硫酸铜溶液中,会得到单质铜,同时生成硫酸亚铁,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;铁的表面出现红色固体.
(5)铁片放在稀硫酸中反应生成硫酸亚铁和氢气,反应的化学方程式为;反应后溶液颜色呈浅绿色.
故答案为:(1)3Fe+2O2
Fe3O4;化合反应;(2)2CO+O2
2CO2;放热;(3)NH4HCO3
NH3↑+CO2↑+H2O;阴凉处密封;(4)Fe+CuSO4═FeSO4+Cu;红;(5)Fe+H2SO4═FeSO4+H2↑;浅绿.
| ||
(2)一氧化碳在空气中燃烧生成二氧化碳,反应的化学方程式为:2CO+O2
| ||
(3)碳酸氢铵易分解产生氨气、水和二氧化碳,反应的化学方程式为NH4HCO3
| ||
(4)“曾青得铁则化为铜”说的是将铁放入硫酸铜溶液中,会得到单质铜,同时生成硫酸亚铁,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu;铁的表面出现红色固体.
(5)铁片放在稀硫酸中反应生成硫酸亚铁和氢气,反应的化学方程式为;反应后溶液颜色呈浅绿色.
故答案为:(1)3Fe+2O2
| ||
| ||
| ||
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
60℃时,A、B两种物质的溶解度A<B.分别取60℃时等质量的A、B两种物质的饱和溶液,降温至30℃,析出A、B晶体的质量分别为m g和n g(A、B均不含结晶水).下列判断正确的是( )
| A、30℃时,A、B两种物质的溶解度一定为A<B |
| B、30℃时,A、B饱和溶液中溶质的质量分数一定为A=B |
| C、30℃时,若溶解度A>B,则晶体质量一定为m<n |
| D、30℃时,若溶解度A<B,则晶体质量一定为m>n |
下列化学方程式书写正确的是( )
A、H2+O2
| ||
| B、H2SO4+NaOH→NaSO4+H2O | ||
| C、CuSO4+2NaOH→Cu(OH)2+2H2O | ||
D、2KMnO4
|
下列有关水的说法错误的是( )
| A、用肥皂水可以区分硬水和软水 |
| B、通过过滤可以除去水中所有的杂质 |
| C、水中异味可用活性炭吸附 |
| D、生活中可以用煮沸的方法降低水的硬度 |
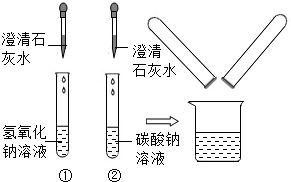 在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等级为同学进行了如图所示实验.
在化学实验技能考试中,有一题目是鉴别碳酸钠溶液和氢氧化钠溶液,小红等级为同学进行了如图所示实验.