题目内容
13.粗盐中有较多的可溶性杂质和不溶性杂质,在粗盐提纯实验中,四次使用玻璃棒,所起的作用分别是:(1)溶解时,使用玻璃棒搅拌,起加快粗盐的溶解速率作用;
(2)过滤时,用玻璃棒引流,使液体沿玻璃棒缓缓流进过滤器;
(3)蒸 发 时,用玻璃棒搅拌,防止局部温度过高,造成液体飞溅;
(4)计算产率时,用玻璃棒将氯化钠晶体从蒸发皿转移出来称量.
分析 (1)根据溶解时玻璃棒的作用,进行分析解答.
(2)根据过滤液体时,注意“一贴、二低、三靠”的原则,进行分析解答.
(3)根据蒸发操作中玻璃棒的作用,进行分析解答.
(4)根据玻璃棒在转移中的作用,进行分析解答.
解答 解:粗盐的主要成分是氯化钠,粗盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程).
(1)溶解时,使用玻璃棒进行搅拌,加快粗盐的溶解速率.
(2)过滤时,用玻璃棒进行引流,使液体沿玻璃棒缓缓流进过滤器.
(3)蒸发时,用玻璃棒搅拌,防止局部温度过高,造成液体飞溅.
(4)计算产率时,用玻璃棒将氯化钠晶体从蒸发皿中转移出来称量.
故答案为:(1)搅拌;加快粗盐的溶解速率;(2)过滤;引流;(3)局部温度过高,造成液体飞溅;(4)转移.
点评 本题难度不大,掌握粗盐提纯的步骤、各步骤中玻璃棒的作用是正确解答本题的关键.

练习册系列答案
相关题目
3.在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应的认识不正确的是( )
| 物质 | X | Y | Z | W |
| 反应前的质量(g) | 2 | 1 | 16 | 16 |
| 反应后的质量(g) | 17 | m | 6 | 11 |
| A. | 物质Y可能是该反应的催化剂 | B. | 该反应为化合反应 | ||
| C. | 反应中Z和X的质量比为3:2 | D. | 反应的Z和W的质量比为2:1 |
4.实验室收集下列气体,一般只用向上排空气法收集,而不用排水法收集的是( )
| A. | O2 | B. | H2 | C. | CO | D. | CO2 |
1.将下列四种物质分别放入水中,能形成溶液的是( )
| A. | 泥土 | B. | 植物油 | C. | 蔗糖 | D. | 汽油 |
18. 小军见到一种“化学爆竹”(见图)只要用手拍打锡纸袋,掷在地上,锡纸袋随后就会突然爆开并伴随响声.他认为,这是锡纸袋中的物质发生化学反应生成气体造成的,于是想探究锡纸袋中的物质成分.
小军见到一种“化学爆竹”(见图)只要用手拍打锡纸袋,掷在地上,锡纸袋随后就会突然爆开并伴随响声.他认为,这是锡纸袋中的物质发生化学反应生成气体造成的,于是想探究锡纸袋中的物质成分.
【提出问题】锡纸袋中的物质是什么?
【查阅资料】主要内容如下.
①过氧化氢分解生成氧气,化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②活泼金属与酸反应生成氢气,例如镁与稀硫酸反应生成氢气,化学方程式为Mg+H2SO4=MgSO4+H2↑.
③含有碳酸根或碳酸氢根的盐与酸反应生成二氧化碳.
【猜想与验证】小军打开一个未用过的锡纸袋,内有一包无色液体和一些白色固体.
(1)猜想:无色液体为酸.
验证:在两支试管中分别加入2mL水和该无色液体,各滴加3滴紫色石蕊试液.紫色石蕊试液遇水不变色,遇该无色液体变红.
试验的初步结论:无色液体为酸. 小军取两试管进行实验的目的是作空白实验,进行对比.
(2)猜想:白色固体为含有碳酸根或碳酸氢根的盐.
验证:请你运用初中所学知识,帮助小军完成下列实验报告.
小军为进一步验证自己的初步结论,继续查找资料,得到下表.
根据上表数据,该白色固体的检验方法是20℃时,在100g水中加入11g该白色固体,充分溶解后,若有白色固体剩余,为碳酸氢钠;否则为碳酸钠.
【反思】通过该探究实验,你还想学习的知识是碳酸钠和碳酸氢钠化学性质上有哪些差异.
 小军见到一种“化学爆竹”(见图)只要用手拍打锡纸袋,掷在地上,锡纸袋随后就会突然爆开并伴随响声.他认为,这是锡纸袋中的物质发生化学反应生成气体造成的,于是想探究锡纸袋中的物质成分.
小军见到一种“化学爆竹”(见图)只要用手拍打锡纸袋,掷在地上,锡纸袋随后就会突然爆开并伴随响声.他认为,这是锡纸袋中的物质发生化学反应生成气体造成的,于是想探究锡纸袋中的物质成分.【提出问题】锡纸袋中的物质是什么?
【查阅资料】主要内容如下.
①过氧化氢分解生成氧气,化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②活泼金属与酸反应生成氢气,例如镁与稀硫酸反应生成氢气,化学方程式为Mg+H2SO4=MgSO4+H2↑.
③含有碳酸根或碳酸氢根的盐与酸反应生成二氧化碳.
【猜想与验证】小军打开一个未用过的锡纸袋,内有一包无色液体和一些白色固体.
(1)猜想:无色液体为酸.
验证:在两支试管中分别加入2mL水和该无色液体,各滴加3滴紫色石蕊试液.紫色石蕊试液遇水不变色,遇该无色液体变红.
试验的初步结论:无色液体为酸. 小军取两试管进行实验的目的是作空白实验,进行对比.
(2)猜想:白色固体为含有碳酸根或碳酸氢根的盐.
验证:请你运用初中所学知识,帮助小军完成下列实验报告.
| 主要实验装置 | 主要操作步骤 | 主要实验现象 | 实验操作目的 |
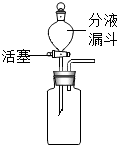 | 在瓶中加入少量白色固体,再加入适量水,振荡,静置 | 白色固体溶解 | 验证白色固体 是否可溶 |
| ①在分液漏斗中加入稀盐酸.塞上胶塞,打开活塞,放出适量溶液后,关闭活塞. ②将气体通入澄清石灰水 | ①大量气泡产生 ②澄清石灰水变浑浊 | 验证生成气体的成分 | |
| 实验的初步结论:白色固体是可溶性碳酸盐,可能为碳酸钠或碳酸氢钠. | |||
| 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
【反思】通过该探究实验,你还想学习的知识是碳酸钠和碳酸氢钠化学性质上有哪些差异.
 如图是市售某品牌牙膏包装盒上的部分说明.其主要活性成分单氟磷酸钠(Na2PO3F)是牙膏的常用添加剂之一,试验表明牙膏中单氟磷酸钠的质量分数 达到0.76%~0.80%时,防龋齿的效果较好.单氟磷酸钠的相对分子质量是144,其中F元素的质量分数为13.19%.该牙膏中单氟磷酸钠的质量分数为0.785%,经判断该牙膏有(填“有”或“无”)较好的防龋齿效果.(结果保留小数点后二位)
如图是市售某品牌牙膏包装盒上的部分说明.其主要活性成分单氟磷酸钠(Na2PO3F)是牙膏的常用添加剂之一,试验表明牙膏中单氟磷酸钠的质量分数 达到0.76%~0.80%时,防龋齿的效果较好.单氟磷酸钠的相对分子质量是144,其中F元素的质量分数为13.19%.该牙膏中单氟磷酸钠的质量分数为0.785%,经判断该牙膏有(填“有”或“无”)较好的防龋齿效果.(结果保留小数点后二位)