题目内容
11.二氧化硫是一种无色具有刺激性气味的气体,它进入大气后可形成硫酸型酸雨.(1)煤、石油、木柴中都含有硫元素,点燃后均会产生二氧化硫气体,可用高锰酸钾溶液检验该气体的存在.
(2)为减少大气污染,火力发电厂采用以下两种方法吸收废气中的二氧化硫.
①用氨水吸收废气中的二氧化硫,其反应原理可用化学方程式表示为4NH3•H2O+2SO2+O2=2(NH4)2SO4+2H2O或2NH3•H2O+2SO2+O2=2NH4HSO4.已知:亚硫酸盐不稳定,易被空气中的氧气氧化成硫酸盐.
②用石灰石浆吸收废气中的二氧化硫,其反应原理是:2CaCO3+2SO2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2CO2.若1000kg废气中含有1.6kg的二氧化硫,则至少需要含90%碳酸钙的石灰石多少千克才能将其完全吸收(写出解题过程,计算结果保留一位小数)?
分析 (1)根据二氧化硫能使高锰酸钾溶液褪色解答;
(2)化学方程式的书写,并且根据化学方程式的计算解答;
解答 解:(1)故答案为:高锰酸钾;
(2)用氨水吸收废气中的二氧化硫,发生的反应是:氨水和二氧化硫和氧气反应生成硫酸铵和水或氨水和二氧化硫和氧气反应生成硫酸氢铵,配平即可;故答案为:①4NH3•H2O+2SO2+O2=2(NH4)2SO4+2H2O或2NH3•H2O+2SO2+O2=2NH4HSO4;
②设至少需要含90%的碳酸钙的石灰石的质量为x
2CaCO3+O2+2SO2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2CO2
200 128
90%•x 1.6kg
$\frac{200}{128}=\frac{90%•x}{1.6kg}$ x=2.8kg;
答:至少需要含90%的碳酸钙的石灰石的质量为2.8kg;
故答案为:2.8kg.
点评 本考点考查了气体的检验方法,又结合了根据化学方程式的计算等,属于难度比较大的题,也是学生经常出错的题型.综合性比较强,并认真分析,综合把握,从而突破本难点.

练习册系列答案
相关题目
2.下列物质充分反应后所得溶液质量比反应前总质量减小的是( )
| A. | 氧化铁加入稀盐酸中 | B. | 硫酸铜溶液和氯化钡溶液混合 | ||
| C. | 氢氧化钠溶液和稀硫酸混合 | D. | 三氧化硫通入氢氧化钠溶液中 |
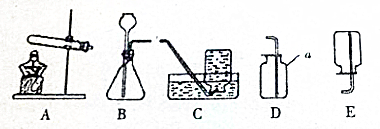
19.如图1是实验室常用的实验仪器与装置,根据所学知识回答下列问题:
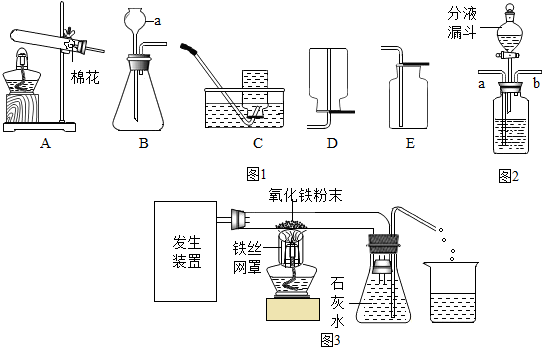
(1)仪器a的名称是长颈漏斗.
(2)实验室用A装置制取氧气的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,为检查A装置的气密性,保持装置内温度不变,将导管的末端伸入装有水的烧杯中,若装置气密性良好,烧杯内导管中的现象(画圈部分)是A.
(3)实验室制取二氧化碳的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,收集装置可选E.
小海用如图2装置验证二氧化碳与水的反应,为说明使石蕊变色的物质是碳酸而不是水或二氧化碳,应该采取的实验操作顺序是②③①④③(填序号)
①从b端通入氮气
②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中
③从a端通二氧化碳
④从分液漏斗中滴加适量水
(4)小露同学利用草酸钠固体(化学式为Na2C2O4)加热分解制取一氧化碳,并用CO还原氧化铁.他设计的实验装置图3:
①一氧化碳的发生装置可以选择上述所给装置中的A(填序号)
②硬质玻璃管中的反应现象是红色固体变成黑色.
③该装置中锥形瓶(足量澄清石灰水)的作用是:
Ⅰ检验并吸收生成的CO2;
Ⅱ收集未反应的一氧化碳,防止污染空气.

(1)仪器a的名称是长颈漏斗.
(2)实验室用A装置制取氧气的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,为检查A装置的气密性,保持装置内温度不变,将导管的末端伸入装有水的烧杯中,若装置气密性良好,烧杯内导管中的现象(画圈部分)是A.
| 选项 | A | B | C | D | 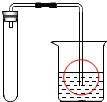 |
| 现象放大图 | 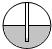 | 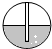 |  | 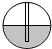 |
小海用如图2装置验证二氧化碳与水的反应,为说明使石蕊变色的物质是碳酸而不是水或二氧化碳,应该采取的实验操作顺序是②③①④③(填序号)
①从b端通入氮气
②将用石蕊溶液染成紫色的干燥纸花放入广口瓶中
③从a端通二氧化碳
④从分液漏斗中滴加适量水
(4)小露同学利用草酸钠固体(化学式为Na2C2O4)加热分解制取一氧化碳,并用CO还原氧化铁.他设计的实验装置图3:
①一氧化碳的发生装置可以选择上述所给装置中的A(填序号)
②硬质玻璃管中的反应现象是红色固体变成黑色.
③该装置中锥形瓶(足量澄清石灰水)的作用是:
Ⅰ检验并吸收生成的CO2;
Ⅱ收集未反应的一氧化碳,防止污染空气.
16.环境保护是我国是一项基本国策.下列行为有利于环境保护的是( )
| A. | 焚烧废弃塑料 | B. | 深埋处理废旧电池 | ||
| C. | 控制企业排污 | D. | 丢弃实验剩余药品 |
3.下列各组物质中,能相互反应且反应前后溶液总质量增加的是( )
| A. | 铁和硫酸铜溶液 | B. | 氧化铁固体和稀硫酸 | ||
| C. | 盐酸和澄清石灰水 | D. | 氯化钠溶液和硝酸钾溶液 |
20.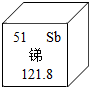 我市盛产金属锑.如图是锑元素在元素周期表中的部分信息,下列有关说法不正确的是( )
我市盛产金属锑.如图是锑元素在元素周期表中的部分信息,下列有关说法不正确的是( )
 我市盛产金属锑.如图是锑元素在元素周期表中的部分信息,下列有关说法不正确的是( )
我市盛产金属锑.如图是锑元素在元素周期表中的部分信息,下列有关说法不正确的是( )| A. | 锑元素属于金属元素 | B. | 锑元素的相对原子质量是121.8g | ||
| C. | 锑原子核外有51个电子 | D. | 锑元素的原子序数为51 |
1.宜昌民生热词:“舌尖上的安全”,下列做法符合食品安全要求的是( )
| A. | 用碳酸氢钠作发酵粉 | B. | 用霉变油菜籽生产食用油 | ||
| C. | 用亚硝酸钠代替食盐烹调食物 | D. | 用工业酒精勾兑饮用白酒 |