题目内容
7.从事科学实验的重要环节是进行科学实验的设计.科学实验的正确步骤应为:①明确实验目的②收集有关资料③设计合理方案④进行科学实验.请你按照以上四步,完成以下实验设计,(所用装置图用序号表示)在实验室中,常用加热固体NH4Cl和Ca(OH)2混合物的方法制取氨气,反应生成 CaCl2、H2O和NH3.已知在标准状况下,氨气的密度为0.77l g/L,空气的密度为l.293g/L,且在常温常压下,l体积水能溶解700体积的氨气.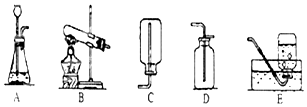
(1)收集有关资料:氨气的密度小于空气密度,且极易溶于水.NH4Cl和Ca(OH)2混合制取氨气的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O.
(2)设计合理方案:发生装置选用B,收集装置选用C.
(3)若实验室用双氧水制氧气,发生装置选用A.
分析 (1)根据相关方面的资料可以确定实验的发生装置和收集装置;
(2)实验室制取氨气需要加热,应该用固体加热型装置作为发生装置;氨气极易溶于水,不能用排水法收集,密度比空气小,可以用向下排空气法收集解答;
(3)根据反应物的状态和反应条件确定反应的发生装置解答;
解答 解:
(1)根据提供的信息可知,反应物NH4Cl和Ca(OH)2都是固体;反应条件是加热;生成的NH3是一种密度小于空气且极易溶于水的气体.反应的方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(2)实验室制取氨气需要加热,应该用固体加热型装置作为发生装置;
氨气极易溶于水,不能用排水法收集,密度比空气小,可以用向下排空气法收集.
(3)用双氧水和二氧化锰制取氧气,可当做固液反应制取气体,反应不需要加热,发生装置选用 A.
故答案为:
(1)小于;极易溶于;2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(2)B;C;
(3)A.
点评 本题考查实验室制取氨气的装置选择和根据化学方程式进行计算,计算时要注意规范性和准确.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
17.下列叙述正确的是( )
| A. | 卢瑟福建立的“卢瑟福模型”认为电子像云雾一样出现在原子核周围 | |
| B. | 汤姆生建立的“汤姆生模型”认为原子核像太阳,电子像行星绕原子核运行 | |
| C. | 玻尔建立的“分层模型”认为电子在原子核周围分层运动 | |
| D. | 现代科学家认为电子像西瓜籽似地嵌在原子中 |
18. 如图是某化学反应前后反应物与生成物分子及其数目变化微观示意图,其中不同的圆球代表不同的原子.下列说法正确的是( )
如图是某化学反应前后反应物与生成物分子及其数目变化微观示意图,其中不同的圆球代表不同的原子.下列说法正确的是( )
 如图是某化学反应前后反应物与生成物分子及其数目变化微观示意图,其中不同的圆球代表不同的原子.下列说法正确的是( )
如图是某化学反应前后反应物与生成物分子及其数目变化微观示意图,其中不同的圆球代表不同的原子.下列说法正确的是( )| A. | 该反应属于分解反应 | |
| B. | 该反应中,参加反应的两种分子个数比为5:1 | |
| C. | 反应前后,原子的种类与数目都发生了改变 | |
| D. | 该反应中,生成物是一种化合物 |
12.下列有关物质(主要成分)的名称、俗称、化学式三者不能表示同一种物质的是( )
| A. | 氯化钠 食盐 NaCl | B. | 甲烷 沼气 CH4 | ||
| C. | 氢氧化钠 纯碱 NaOH | D. | 氢氧化钙 熟石灰 Ca(OH)2 |
16.以下四种反应物,其中不能直接通过与稀硫酸反应制得MgSO4的是( )
| A. | Mg | B. | MgO | C. | MgCl2 | D. | Mg(OH)2 |
17.下列物质的俗名与化学式相符合的一组是( )
| A. | 熟石灰 CaO | B. | 生石灰 CaCO3 | C. | 烧碱 NaOH | D. | 草木灰 Ca(OH)2 |