题目内容
某学校化学兴趣小组的同学想测定某建筑工地大理石中碳酸钙的含量,做了如下实验:首先称取50g该大理石样品放入烧杯中,然后将200g的稀盐酸分5次加入烧杯内(假设其余杂质均不与盐酸反应也不溶于水)进行充分反应.实验过程中的数据记录如下:
请回答下列问题:
(1)该小组同学要用质量分数为36.5%浓盐酸配制所需的200克稀盐酸,则需浓盐酸的质量为多少?
(2)求一共生成二氧化碳质量?
(3)向第二次反应后所得溶液中加8.8g水,则所得溶液的溶质质量分数?
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 稀盐酸的质量 | 40g | 40g | 40g | 40g | 40g |
| 剩余固体质量 | 40.0g | X | 20.0g | 10.0g | 5.0g |
(1)该小组同学要用质量分数为36.5%浓盐酸配制所需的200克稀盐酸,则需浓盐酸的质量为多少?
(2)求一共生成二氧化碳质量?
(3)向第二次反应后所得溶液中加8.8g水,则所得溶液的溶质质量分数?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据第一次加入40g稀盐酸,导致固体由50g变成了40g,减少了10g,第三次也是有20g变成10g,说明每加入40g盐酸能够使固体减少10g,依据杂质不与盐酸反应,反应的是碳酸钙,结合方程式计算出所用稀盐酸溶质的质量分数,并据溶质的质量分数式分析解答;
(2)第5次加入40g盐酸,固体减少5g,说明样品中碳酸钙反应完毕,依据碳酸钙的总质量计算生成的二氧化碳的总质量即可;
(3)利用第二次实验所消耗碳酸钙的量,根据反应的化学方程式,计算出生成的氯化钙的质量,由溶质的质量分数公式,求出加入水后溶液中溶质的质量分数.
(2)第5次加入40g盐酸,固体减少5g,说明样品中碳酸钙反应完毕,依据碳酸钙的总质量计算生成的二氧化碳的总质量即可;
(3)利用第二次实验所消耗碳酸钙的量,根据反应的化学方程式,计算出生成的氯化钙的质量,由溶质的质量分数公式,求出加入水后溶液中溶质的质量分数.
解答:解:(1)第一次加入40g稀盐酸,导致固体由50g变成了40g,减少了10g,第三次也是有20g变成10g,说明每加入40g盐酸反应10g碳酸钙
设反应10g碳酸钙需要盐酸溶质的质量是y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
10g y
=
解得y=7.3g
40g稀盐酸含有溶质的质量是7.3g,则200g稀盐酸中含有溶质的质量是7.3g×5=36.5g;
需要浓盐酸的质量是
=100g;
(2)要求生成二氧化碳的总质量,则须求出所有碳酸钙反应生成的二氧化碳的质量,第5次加入40g盐酸,固体减少5g,说明样品中碳酸钙反应完毕,所以碳酸钙的总质量是50g-5g=45g
设45g碳酸钙与盐酸反应生成二氧化碳的总质量是x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
45g x
=
x=19.8g
(3)第二次反应的碳酸钙的质量是20g,设生成的二氧化碳的质量是a,生成氯化钙的质量是b
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
20g b a
=
=
a=8.8g
b=22.2g
所以向第二次反应后所得溶液中加入8.8g水,所得溶液的溶质质量分数是
×100%=22.2%
答:(1)则需浓盐酸的质量为100g;
(2)一共生成二氧化碳质量为19.8g;
(3)向第二次反应后所得溶液中加8.8g水,则所得溶液的溶质质量分数为22.2%.
设反应10g碳酸钙需要盐酸溶质的质量是y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73
10g y
| 100 |
| 10g |
| 73 |
| y |
解得y=7.3g
40g稀盐酸含有溶质的质量是7.3g,则200g稀盐酸中含有溶质的质量是7.3g×5=36.5g;
需要浓盐酸的质量是
| 36.5g |
| 36.5% |
(2)要求生成二氧化碳的总质量,则须求出所有碳酸钙反应生成的二氧化碳的质量,第5次加入40g盐酸,固体减少5g,说明样品中碳酸钙反应完毕,所以碳酸钙的总质量是50g-5g=45g
设45g碳酸钙与盐酸反应生成二氧化碳的总质量是x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
45g x
| 100 |
| 45g |
| 44 |
| x |
x=19.8g
(3)第二次反应的碳酸钙的质量是20g,设生成的二氧化碳的质量是a,生成氯化钙的质量是b
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
20g b a
| 100 |
| 20g |
| 111 |
| b |
| 44 |
| a |
a=8.8g
b=22.2g
所以向第二次反应后所得溶液中加入8.8g水,所得溶液的溶质质量分数是
| 22.2g |
| 20g+80g+8.8g-8.8g |
答:(1)则需浓盐酸的质量为100g;
(2)一共生成二氧化碳质量为19.8g;
(3)向第二次反应后所得溶液中加8.8g水,则所得溶液的溶质质量分数为22.2%.
点评:本题考查综合、全面,分析透彻每次加入40g稀盐酸固体剩余物质量的变化,对反应进行的情况进行判断,这是解决本题的基础,该题可很好考查学生分析、解决问题的能力,本题涉及的方程式计算较多,要找准已知量,细心分析.

练习册系列答案
相关题目
下列变化中,属于化学变化的是( )
| A、冰雪融化 | B、汽油挥发 |
| C、湿衣服晾干 | D、木柴燃烧 |
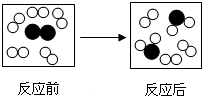 如图是某个化学反应前后的微观模拟图.请根据图示判断参加反应的
如图是某个化学反应前后的微观模拟图.请根据图示判断参加反应的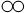 和
和 与反应后生成的
与反应后生成的 个数比( )
个数比( )| A、5:1:2 |
| B、2:3:1 |
| C、1:1:1 |
| D、2:1:2 |
 下图是某品牌补铁剂的标签.
下图是某品牌补铁剂的标签.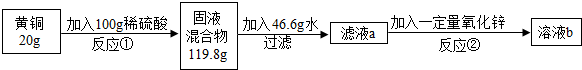
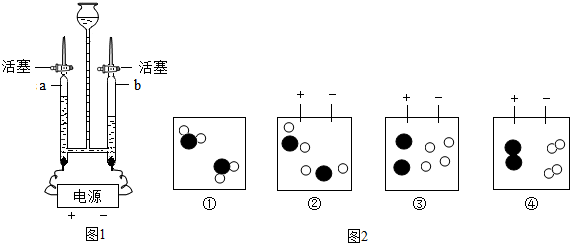
 ”表示氧原子,“
”表示氧原子,“ ”表示氢原子).则从反应开始到完成,微粒运动变化的先后顺序是
”表示氢原子).则从反应开始到完成,微粒运动变化的先后顺序是