题目内容
15.物质发生化学变化的前后,总质量是否发生改变?是增加、减小还是不变呢?甲、乙、丙三位同学按下面的步骤进行探究:(1)提出假设:物质发生化学变化前后总质量不变.
(2)设计并进行实验,甲设计的实验装置和选用的药品如图A所示,乙设计的实验装置和选用药品如图B所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察.
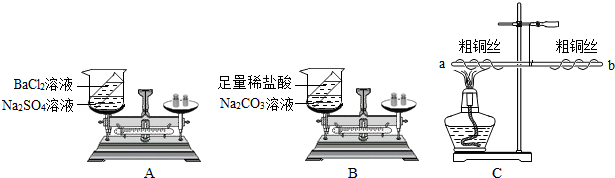
写出A、B两个实验发生反应的化学方程式:BaCl2+Na2SO4═BaSO4↑+2NaCl,Na2CO3+2HCl═2NaCl+CO2↑+H2O.丙进行了图C所示的实验,在一根用细铜丝吊着的长玻璃棒两端,分别绕上粗铜丝,并使玻璃棒保持水平.然后,用酒精灯给a端铜丝加热数分钟.停止加热后冷却,他观察到的现象是a端上的铜丝变黑、玻璃棒a端下沉.
(3)实验结论:
甲认为:在化学反应中,生成物的总质量与反应物的总质量相等;
乙、丙认为:在化学反应中,生成物的总质量与反应物的总质量不相等.
(4)你认为甲的结论正确,请从原子的角度分析,结论正确的理由是:在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变.
(5)导致其他实验结论错误的原因是B实验反应后生成的气体逸散到空气中去了,C实验a端铜丝增加了氧元素的质量.因此,如果有气体参与反应或生成物中有气体的反应,则一定要设计反应在密闭装置中进行.
分析 (2)根据反应物和复分解反应的原理书写化学方程式.铜在加热的条件下会与氧气反应生成氧化铜,会使铜丝质量增加.
(4)化学反应的过程实际上是原子的重新组合过程,原子的数目、质量、种类不会增减.
(5)在验证质量守恒定律时,若有气体参加或生成的实验必须在密闭的环境中进行.
解答 解:(2)由图示可知发生的反应是氯化钡和硫酸钠反应,发生反应的化学方程式为:BaCl2+Na2SO4═BaSO4↑+2NaCl;
根据反应物是碳酸钠和盐酸及复分解反应的原理可知,生成物是氯化钠、水和二氧化碳,故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
铜在加热的条件下会与氧气反应生成黑色的氧化铜,会使铜丝质量增加,会使左端下沉,故答案为:a端上铜丝变黑;玻璃棒a端下沉
(4)化学反应的过程实际上是原子的重新组合过程,原子的数目、质量、种类不会增减,故答案为:
甲⑥在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变
(5)在验证质量守恒定律时,若有气体参加或生成的实验必须在密闭的环境中进行,生成物的质量等于参加的反应物的质量之和,故答案为:
B实验反应后生成的气体逸散到空气中去了
C实验a端铜丝增加了氧元素的质量
有气体参与反应或者生成物中有气体
答案:
(2)BaCl2+Na2SO4═BaSO4↑+2NaCl; Na2CO3+2HCl═2NaCl+CO2↑+H2O;a端上的铜丝变黑; 玻璃棒a端下沉.
(4)甲;在化学反应中,反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变;
(5)B实验反应后生成的气体逸散到空气中去了; C实验a端铜丝增加了氧元素的质量;有气体参与反应或生成物中有气体.
点评 在验证质量守恒定律时,有气体参加的实验必须密封,若不密封所得的生成物的质量与反应物的质量不相等,不能得出质量守恒的结论.

 阅读快车系列答案
阅读快车系列答案| A. |  检查装置气密性 | B. |  给试管内液体加热 | ||
| C. |  铁丝在氧气中燃烧 | D. | 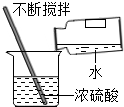 稀释浓硫酸 |
| A. | 打开浓硫酸瓶盖,产生白雾 | |
| B. | 电解水正极产生的气体是氧气 | |
| C. | 氨气能使湿润的红色石蕊试纸变蓝 | |
| D. | 硝酸铵固体溶于水中,溶液温度升高 |
| 物质 | A | B | C | D |
| 反应前的质量/g | 10 | 162 | 8 | 3.8 |
| 反应后的质量/g | 0.2 | X | 0 | 18 |
| A. | X的值为165.6 | |
| B. | 该反应可能为复分解反应 | |
| C. | 反应过程中,B与D的质量比为18:71 | |
| D. | 若A与C的相对分子质量之比为49:20,则A与C的化学计量数比为2:1 |
| A. | 白醋 | B. | 蔗糖 | C. | 香油 | D. | 食盐 |
| A. | ClO4- | B. | ClO3- | C. | ClO2- | D. | ClO- |




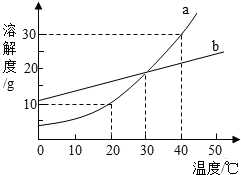 如图是a、b两种固体物质的溶解度曲线.
如图是a、b两种固体物质的溶解度曲线.