题目内容
13.镉是一种重金属元素,人体内重金属超标会抑制钙吸收,使人易患骨质疏松、骨痛病.高温下镉可与硫直接化合生产硫化镉.氢氧化镉的溶解度很小.阅读材料回答以下问题: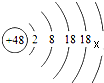
(1)如图是镉(Cd)原子结构图,其中x为2,在化学反应中镉原子容易失去(填“得到”或“失去”)电子,形成的离子符号可表示为Cd2+.
(2)请标出氢氧化镉[Cd(OH)2]中镉元素的化合价$\stackrel{+2}{Cd}(OH)_{2}$.
(3)写出镉与硫化合的化学方程式:Cd+S$\frac{\underline{\;高温\;}}{\;}$CdS.
分析 (1)根据在原子中质子数=核外电子数;最外层电子数小于4的原子易失去电子形成离子;
(2)根据化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后解答;
(3)高温下镉可与硫直接化合生成硫化镉解答.
解答 解:
(1)在原子中质子数=核外电子数;故x=48-2-8-18-18=2;最外层电子数为2,易失去最外层的电子形成带两个单位正电荷的镉离子;故填:2;失去电子;Cd2+;
(2)化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后.氢氧化镉[Cd(OH)2]中镉元素的化合价表示为:$\stackrel{+2}{Cd}(OH)_{2}$
(3)高温下镉可与硫直接化合生成硫化镉,化学方程式为:Cd+S$\frac{\underline{\;高温\;}}{\;}$CdS.
答案:
(1)2;失去电子;Cd2+;
(2)$\stackrel{+2}{Cd}(OH)_{2}$
(3)Cd+S$\frac{\underline{\;高温\;}}{\;}$CdS.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
8.在实验室掌握正确的操作方法至关重要,下列实验操作正确的是( )
| A. | 加热后的试管,倒掉废液后立即用冷水冲洗 | |
| B. | 为了节约实验时间.可以随时向燃着的酒精灯内添加酒精 | |
| C. | 实验室制取C02时,先使试管倾斜,再用药匙取较大块大理石小心送至试管底部 | |
| D. | 量液时,量筒先放平,视线与液体凹面的最低处保持水平,再读数 |
18.小明欲探究某氢氧化钠溶液的变质程度,他取100g溶液,往其中分四次滴入100g某稀盐酸,其产生气体的总质量与滴入盐酸的关系如表所示:
(1)碳酸钠中碳元素的质量分数:11.3%(精确到0.1%)
(2)第一次滴入盐酸没气体产生的原因是:盐酸先与溶液中的氢氧化钠反应而不产生气体;
(3)求100g变质的氢氧化钠溶液中碳酸钠的质量.(写出计算过程)
| 次数 | 1 | 2 | 3 | 4 |
| 滴入稀盐酸的质量 | 25g | 25g | 25g | 25g |
| 产生气体的总质量 | 0 | 1.1g | 3.3g | 3.3g |
(2)第一次滴入盐酸没气体产生的原因是:盐酸先与溶液中的氢氧化钠反应而不产生气体;
(3)求100g变质的氢氧化钠溶液中碳酸钠的质量.(写出计算过程)
5.下列过程中,发生化学变化的是( )
| A. | 食物腐败 | B. | 酒精挥发 | C. | 水结冰 | D. | 海水晒盐 |
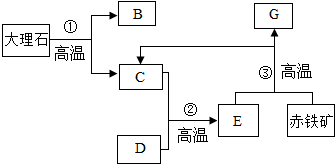 工业上以大理石和赤铁矿为主要原料制取B和G,其转化关系如图所示,已知D、G为单质.回答下列问题:
工业上以大理石和赤铁矿为主要原料制取B和G,其转化关系如图所示,已知D、G为单质.回答下列问题: