题目内容
将一定量的锌粉和铁粉同时放入硫酸铜溶液中,充分反应后,过滤得滤渣和无色滤液.
(1)滤液中大量存在的阳离子是 (用化学用语表示);
(2)滤渣中一定有 ;
(3)请写出一个该实验过程中发生反应的化学方程式: .
(1)滤液中大量存在的阳离子是
(2)滤渣中一定有
(3)请写出一个该实验过程中发生反应的化学方程式:
考点:金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据金属的活动性顺序表的应用可知,三种金属的活动性由强到弱的顺序:锌>铁>铜,依据实验现象“得到无色溶液”,判断铁、锌混合物与硝酸铜充分反应的结果.
解答:解:由金属活动性顺序的应用及题意可知,充分反应后溶液为无色,此现象可说明铁和硝酸铜没有发生反应;因为锌活动性大于铁,可知在铁开始与硝酸铜反应时锌已经把硝酸铜反应完,则滤出的固体中一定含铁和铜,而滤液中一定含硝酸锌.发生反应的化学方程式:Zn+CuSO4═Cu+ZnSO4
答案:
(1)Zn2+
(2)Fe和Cu
(3)Zn+CuSO4═Cu+ZnSO4
答案:
(1)Zn2+
(2)Fe和Cu
(3)Zn+CuSO4═Cu+ZnSO4
点评:金属混合粉末放入盐溶液时,活动性强的金属先与盐发生反应,待活动性强的金属完全反应后活动性弱的金属开始反应.

练习册系列答案
相关题目
“酒驾”已经写入刑法.人体血液中酒精含量超过80mg/100mL为酒驾.交警常使用一种“酒精检测仪”检测司机是否酒后驾车.其反应原理为CH3CH2OH+4CrO3+6H2SO4═2X+CO2↑+9H2O,则X的化学式为( )
| A、Cr2O3 |
| B、CrSO4 |
| C、Cr2(SO4)3 |
| D、Cr2S3 |
如图所示操作中,正确的是( )
A、 熄灭酒精灯 |
B、 添加药品 |
C、 过滤 |
D、 量取35mL液体 |
分类法是化学学习和研究的重要方法之一.下列分类正确的是( )
| A、金属元素:金刚石、水银、铅 |
| B、氧化物:双氧水、冰、酒精 |
| C、混合物:空气、石油、石灰石 |
| D、清洁能源:氢气、太阳能、汽油 |
化学与人体健康的关系十分密切.下列做法中不会危及人体健康的是( )
| A、用小苏打做糕点的疏松剂 |
| B、用过量添加剂增白面粉 |
| C、用甲醛浸泡海产品保鲜 |
| D、用工业盐亚硝酸钠腌渍鱼肉 |
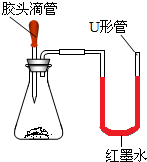 化学是一门以实验为基础的科学.根据下列实验回答问题.
化学是一门以实验为基础的科学.根据下列实验回答问题.