题目内容
5.“碳铵”(NH4HCO3)是一种常用的化学肥料,易溶于水,受潮时在常温下就能分解,温度越高分解越快,分解产物为NH3、CO2、H2O.“碳铵”遇碱放出氨气,在土壤中不残留有害物质.(1)“碳铵”属于化肥中的氮肥,化学性质不稳定(填“稳定”或“不稳定”);保存时应
注意①②.(选填序号)
①贮存和运输时要密封,不要受潮和曝晒;施用后要立即盖土或立即灌溉
②不要与碱性物质混放或混用
③不能与易燃物质混在一起;结块时,不要用铁锤砸碎
④不宜长期施用
某兴趣小组欲在实验室利用如图所示的装置研究“碳铵”的部分性质,请你一起参与.
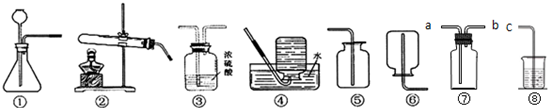
(2)选择装置②(填序号)进行“碳铵”固体受热分解的实验,该反应的化学方程式为NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O;应用该装置,还可以在实验室进行的实验是实验室用高锰酸钾加热制取氧气.(答一个即可)
(3)利用装置①,写出实验室制取一种气体的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O,收集该气体的装置应选择⑤.
(4)取少量“碳铵”和熟石灰粉末放入装置②的大试管中,微热片刻立即移开酒精灯.将产生的氨气缓缓通入盛有酚酞试液的试管中,酚酞试液变红.
①由此可知,氨气易溶于水,其水溶液(氨水)显碱性(填“酸”、“碱”或“中”),pH>7(填“<”、“>”或“=”).
②某同学认为可用装置③干燥氨气你认为他能否达到目的?简要分析原因.不能,因为氨气能与浓硫酸发生化学反应而被吸收;
③由于氨气具有强烈的刺激性气味,对人体的呼吸道粘膜有较大的伤害,我们可以选用上述的装置中的⑦和⑧连接收集并吸收逸散出来的多余氨气,则应将a(选填“a”或“b”)与c相连接,烧杯中应盛放水或某种酸液.
分析 (1)根据化肥所提供作物生成元素把化肥分为:提供N元素的氮肥,提供P元素的磷肥,提供K元素的钾肥,提供N、P、K三种中两种或以上元素的复合肥;根据“碳铵”(NH4HCO3)的化学式确定碳铵为氮肥;由于碳酸在常温下就能分解且温度越高分解越快,可判断碳铵化学性质不稳定,保存时应避免曝晒;由于铵根遇碱释放出氨气而降低肥效,保存要应避免与碱性物质共存;
(2)装置②适用于对固体加热产生气体的反应,进行“碳铵”固体受热分解的实验宜采用该装置;碳铵受热时发生分解反应,可生成氨气、水和二氧化碳;实验室通过采取加热高锰酸钾或氯酸钾制取氧气,在加热固体高锰酸钾或氯酸钾制氧气时也可采取装置②;
(3)装置①适用于固体与液体常温下反应制取气体,因此,利用碳酸钙与盐酸、锌与硫酸、过氧化氢与二氧化锰制取二氧化碳、氢气、氧气时可选用该装置;在收集气体时,氧气、二氧化碳密度比空气的大可选择⑤向上排空气法收集,氢气密度小于空气可选择⑥向下排空气法收集,氧气、氢气难溶于水可选择④排水法收集;
(4)①酚酞试液变红,说明氨水呈碱性,碱性溶液pH大于7;
②装置③内盛放浓硫酸,浓硫酸可与氨气反应生成硫酸铵,不能用于干燥氨气;
③氨气密度小于空气应排取向下支收集,因此,采取装置⑦收集氨气时,氨气应从b管进入使瓶内空气由下部的a管排出;氨气极易溶于水或与酸溶液发生反应,因此可在烧杯内放水或酸溶液吸收多余的氨气.
解答 解:(1)根据“碳铵”(NH4HCO3)的化学式可知碳铵可提供作物生成所需的N元素,因此应属于氮肥;
由于碳酸在常温下就能分解且温度越高分解越快,因此推断碳铵化学性质不稳定;
碳铵化学性质不稳定且易潮解,因此在保存、运输时应密封,不要受潮和曝晒等;“碳铵”遇碱放出氨气,在保存时不能与碱性一起存放;
故答案为:氮;不稳定;①②;
(2)进行“碳铵”固体受热分解的实验需要选择适用于加热固体制取气体的装置②;加热过程中,碳铵受热分解生成氨气、水和二氧化碳;该装置还可用于高锰酸钾受热分解制取氧气;
故答案为:②;NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O;实验室用高锰酸钾加热制取氧气;
(3)装置①适用于固体与液体常温下反应制取气体,因此,利用固体碳酸钙与盐酸溶液制取二氧化碳时可选用该装置;在收集气体时,二氧化碳密度比空气的大可选择⑤向上排空气法收集,二氧化碳能溶于水不可选择④排水法收集;
故答案为:CaCO3+2HCl=CaCl2+CO2↑+H2O;⑤;
(4)①产生的氨气缓缓通入盛有酚酞试液的试管中,酚酞试液变红,证明氨水呈碱性,其溶液pH大于7;
故答案为:碱;>;
②氨气能与浓硫酸反应生成硫酸铵而被干燥剂浓硫酸吸收,因此,不能使用浓硫酸干燥氨气;
故答案为:不能,因为氨气能与浓硫酸发生化学反应而被吸收;
③氨气密度小于空气应排取向下支收集,采取装置⑦收集氨气时,氨气应从b管进入使瓶内空气由下部的a管排出;因此,应将a管与c进行连接;为吸收多余的氨气,可在烧杯内放水或酸溶液;
故答案为:a;水或某种酸液.
点评 浓硫酸为酸性干燥剂,只能用于干燥遇水呈酸性的二氧化碳、或遇水呈中性的氢气和氧气等气体;而干燥遇水呈碱性的氨气时,只能选择碱性干燥剂氢氧化钠、碱石灰等,或中性干燥氯化钙等.

| 方案 | 药品 | 实验现象 | 结论 | 反应原理(即方程式) |
| 方案 (取样) | 紫色石蕊试液 | 一支试管中溶液颜色变红色,一支试管溶液颜色变蓝色 | 能使紫色石蕊试液变红色的是稀盐酸,变蓝色的是氢氧化钠溶液 | 紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝 |
①用托盘天平称取5.6g氧化铜粉末
②用容积为10mL的试管盛5mL水在酒精灯上加热
③用排水集气法可得到比较纯净的氧气
④用10mL量筒量取8.2mL水.
| A. | 只有①④ | B. | ①②④ | C. | ①③④ | D. | 只有②③ |
(1)选择药品.小明对三组药品进行了研究,实验记录如下:
| 组别 | 药品 | 实验现象 |
| ① | 块状石灰石和稀盐酸 | 产生气泡速率适中 |
| ② | 块状石灰石和稀硫酸 | 产生气泡速率缓慢并逐渐停止 |
| ③ | 碳酸钠粉末和稀盐酸 | 产生气泡速率很快 |
不选择第③组药品的原因是反应速度太快不利于收集.
(2)选择装置.他选择图中B作为制取的发生装置.你认为他选择的依据是固体和液体发生反应,反应条件是常温,小丽认为利用B装置也可以选择第③组药品来制取二氧化碳,理由是利用分液漏斗控制液体流速,可以控制反应速度.

(3)制取气体.将药品装入所选装置制取气体,并只能用图中D组装置收集.原因是二氧化碳能溶于水,密度比空气大.
(4)气体检验.小明将生成的气体通入石蕊溶液中,溶液变红,因此他确定该气体是二氧化碳.他的检验方法是否正确?不正确请说明理由.因为还有其他气体也可以使紫色石蕊变红色.请写出正确的检验二氧化碳的方法:Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示).
| A. | Fe和Cu | B. | Fe和Ag | C. | Ag | D. | Cu 和Ag |
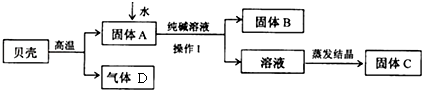
(1)贝壳高温煅烧时,发生反应的化学方程式是CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
(2)固体A和还原铁粉是食品包装袋中常用的两种干燥剂.
①可区分两种干燥剂的简单物理方法是用磁铁吸引;
②操作Ⅰ中用到的玻璃仪器有烧杯、漏斗、玻璃棒;
(3)溶液蒸发结晶得到固体C的过程中,常用玻璃棒搅拌,其目的是使液体受热均匀,防止液滴外溅;
【问题与发现】该小组同学所得到固体C一定是纯净的NaOH吗?
【猜想与假设】根据反应原理,甲、乙、丙三位同学提出以下猜想:
甲:纯净的NaOH;乙:NaOH和Na2CO3的混合物;丙:NaOH和Ca(OH)2的混合物
【探究与验证】甲、乙、丙三位同学分别设计下列方案,对自己的猜想进行验证.他们的实验操作、现象和结论记录如下表,请参与他们的探究并完成所缺内容.
| 实验操作 | 现象 | 结论 | |
| 甲 | 取少量固体C,溶于适量水形成溶液后,滴加几滴酚酞试液 | 溶液变红 | 猜想成立 |
| 乙 | 取少量固体C,溶于适量水形成溶液后,滴加足量稀硫酸 | 无气泡产生 | 猜想不成立 |
| 丙 | 取少量固体C,溶于适量水形成溶液后,滴加几滴饱和碳酸钠溶液 | 出现白色沉淀 | 猜想成立 |
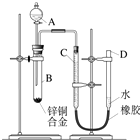 某学习小组用如右图所示装置测定锌铜合金中锌、铜的质量分数.
某学习小组用如右图所示装置测定锌铜合金中锌、铜的质量分数.