题目内容
5.某有机物在氧气中充分燃烧后,产生只有二氧化碳和水,甲、乙两组同学分别用下图两种方法测定它的组成.请你分析,并参与测定工作: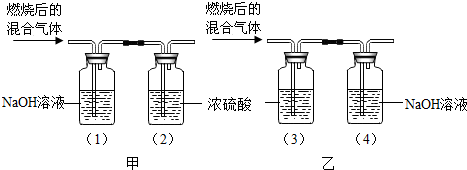
| 燃烧有机物的质量 | 实验装置 | 实验(1)~(4)装置质量 | ||
| 实验前 | 实验后 | |||
| 甲组 | 3.2g | 甲 | (1)150g | (1)154.6g |
| (2)150g | (2)153.4g | |||
| 乙组 | 3.2g | 乙 | (3)150g | (3)153.6g |
| (4)150g | (4)154.4g | |||
(2)根据表中数据,通过计算推测出该有机物是哪些元素组成的?
分析 (1)根据实验装置的作用分析解答:通过浓硫酸质量的增加测定生成水的质量,依据氢氧化钠质量的增加测定生成二氧化碳的量,气体从溶液中出来要带部分水蒸气,故要排除水蒸气的干扰,须先通过浓硫酸,再通过氢氧化钠溶液;
(2)根据质量守恒定律判断有机物中是否含有元素.
解答 解:(1)通过浓硫酸质量的增加测定生成水的质量,依据氢氧化钠质量的增加测定生成二氧化碳的量,气体从溶液中出来要带部分水蒸气,故要排除水蒸气的干扰,须先通过浓硫酸,再通过氢氧化钠溶液,选择B方法;
(2)据质量守恒定律可知反应前后元素种类不变,有机物燃烧生成二氧化碳和水,可知有机物中含有碳元素和氢元素,也就是说生成的水中的氢元素就是有机物中的氢元素,生成的二氧化碳中碳元素的质量就是有机物中碳元素的质量,浓硫酸质量的增加量是生成水的质量,氢氧化钠的质量的增加量就是生成二氧化碳的质量;在检验二氧化碳质量和水的质量时,根据A方法计算:浓硫酸质量增加了3.6g,所以生成水3.6g,则氢元素的质量:3.6g×$\frac{2}{18}$×100%≈0.4g,氢氧化钠溶液质量增加了4.4g,所以生成二氧化碳质量为4.4g,所以碳元素质量为:4.4g×$\frac{12}{44}$×100%≈1.2g,所以碳元素和氢元素质量和为:0.4g+1.2g=1.6g,因为有机物质量为3.2g,所以有机物中还含有氧元素3.2g-1.6g=1.6g.
故答案为:(1)乙; 若先通过氢氧化钠再通过浓硫酸,会影响对原混合气体中水蒸气的测定;
(2)碳、氢、氧.
点评 解答本题的关键是明确浓硫酸质量的增加量就是生成水的质量,氢氧化钠溶液质量的增加量就是生成的二氧化碳的质量,要测定水的质量须先通过浓硫酸,并能据质量守恒定律进行相关的分析和计算.

 快捷英语周周练系列答案
快捷英语周周练系列答案| A. | 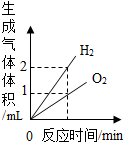 电解水时生成氢气和氧气的体积关系 | |
| B. | 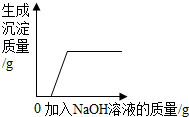 向盐酸和氯化铜的混合物溶液中滴加过量的氢氧化钠溶液 | |
| C. | 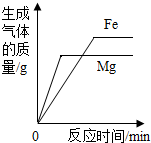 将等质量的镁粉、铁粉分别加入到足量且溶质质量分数相同的稀硫酸中 | |
| D. | 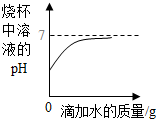 向盛有一定质量稀盐酸的烧杯中不断加水稀释 |
| 操作步骤 | 实验现象 | 结论或化学反应方程式 |
| 取少量样品置于试管中,加入足量稀硫酸,将试管用导管与澄清石灰水相连. | ①产生大量气体,使石灰水变浑浊. ②样品全部溶解,溶液呈蓝色. | ①样品中含有碳酸根离子 ②样品中含有铜离子 |
| 在上述蓝色溶液中,插入一根洁净的铁丝. | ①铁丝表面缓缓产生少量气泡. ②片刻后铁丝表面出现红色物质. | ①Fe+H2SO4═H2↑+FeSO4 ②Fe+CuSO4═Cu+FeSO4 (均用方程式表示) |
为了进一步确定该物质的元素组成,查阅部分资料后,他继续进行了实验.
【资料查阅】白色的无水硫酸铜可做吸水剂,遇水会变成蓝色.
【实验步骤】①如图搭建实验仪器,并检验装置的气密性.
②在A装置中装入11.1g绿色粉末.关闭K1,打开K2、K3,持续通入适量N2.
③关闭K2、K3,分别称量装置B、C、D的质量,记录数据.
④打开K3,点燃酒精灯加热绿色粉末直至装置C中无气泡产生时,关闭K3,熄灭酒精灯.分别称量装置B、C、D的质量,记录数据.
⑤待A冷却后,打开K1、K3,持续通入适量CO,再次点燃酒精灯加热.
⑥当A中粉末全部变红后,熄灭酒精灯.试管冷却后,关闭K1.称量装置A、B、C、D的质量,记录数据.
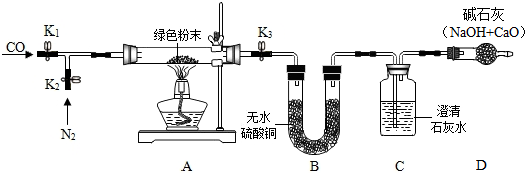
【实验现象和数据处理】
| 装置A | 装置B | 装置C | 装置D | |
| 第一次 加热后 | 绿色粉末变黑色 | 白色粉末变蓝色 质量增加0.9g | 出现白色沉淀, 质量增加2.2g | 无明显变化 质量不改变 |
| 第二次 加热后 | 黑色粉末变红色 质量为6.4g | 无明显变化, 质量不改变 | 沉淀先增加后部分溶解; 质量增加 | 无明显变化 质量不改变 |
(1)老师看了实验方案后认为,从环保的角度来看,此装置有一个缺陷,建议装置D后还应添加一个酒精灯,并在实验步骤⑤ (填实验步骤的序号)中点燃.
(2)步骤②通入氮气的目的是:将试管内的空气排尽,以免其中有物质和绿色粉末反应
【实验结论】
该绿色粉末的组成元素是:Cu、C、O、H;各元素的质量比为:Cu:C:H:O═64:6:1:40(写出计算过程).
| A. | “磨刀不误砍柴工”--减小受力面积,增大压强 | |
| B. | “潭清疑水浅”--光发生了反射 | |
| C. | “花气习人知昼暖”--温度升高,分子的热运动加剧 | |
| D. | “司南之杓,投之于地,其抵指南”--地球周围存在磁场 |
 某化学兴趣小组的同学用如图所示装置进行以下三个实验.
某化学兴趣小组的同学用如图所示装置进行以下三个实验.