题目内容
13.我市某电镀厂为减少水污染及节约成本,从含有CuSO4,MgSO4、FeSO4的废水中回收重要原料MgSO4和有关金属,实验过程如图: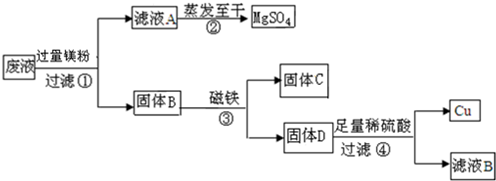
请回答:
(1)滤液A和滤液B含有相同的溶质是MgSO4,因此,可将滤液A和滤液B一起蒸发,其目的是可回收更多的MgSO4.
(2)写出步骤①中反应的化学方程式:Mg+CuSO4=MgSO4+Cu,,Mg+FeSO4=MgSO4+Fe.
(3)步骤①加入的镁粉为什么要过量,请你简要说明理由将废液中的FeSO4和CuSO4完全反应掉.
(4)固体B的物质是Mg、Fe、Cu.
分析 在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,再根据物质之间相互作用时能否发生反应及其反应时生成物是什么等方面进行分析、考虑,从而得出正确的结论.
解答 解:向含有CuSO4,MgSO4、FeSO4的废水中加入过量的镁,镁能先后与硫酸铜和硫酸亚铁反应生了人硫酸镁、铜和铁,通过过滤得到的滤液A中只含有硫酸镁,固体B中含有铜、铁和镁;用磁铁吸附,得到的固体C是铁;固体D是铜和镁,再加入足量稀硫酸,将镁反应生成了硫酸镁,铜不反应过滤即可得到铜.所以:
(1)滤液A和滤液B含有相同的溶质是MgSO4,因此,可将滤液A和滤液B一起蒸发,其目的是:可回收更多的MgSO4.
(2)步骤①中镁先后与硫酸铜、硫酸亚铁发生了反应,反应的化学方程式:Mg+CuSO4=MgSO4+Cu,Mg+FeSO4=MgSO4+Fe.
(3)步骤①加入的镁粉要过量,原因是:将废液中的FeSO4和CuSO4完全反应掉.
(4)固体B的物质是:Mg、Fe、Cu.
故答为:(1)MgSO4,可回收更多的MgSO4;(2)Mg+CuSO4=MgSO4+Cu,Mg+FeSO4=MgSO4+Fe.(3)将废液中的FeSO4和CuSO4完全反应掉;(4)Mg、Fe、Cu.
点评 本题考查金属的回收和废水的利用,学生应明确金属的活泼性来分析发生的化学反应,并应能准确判断每步转化中滤液和固体的成分.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
3.我县淀粉厂排放的废水中含有少量的NaOH、Na2SO4,按环保要求需要把废水处理成pH=7且水中只含有少量NaCl才能排放.则工厂废水处理需要加入的一组物质是( )
| A. | MgSO4、NaCl | B. | BaCl2、HCl | C. | H2SO4、Ba(NO3)2 | D. | H2SO4、MgCl2 |
8.白蚁能分泌出蚁酸.蚁酸的化学性质与盐酸相似,下列物质不与蚁酸反应的是( )
| A. | Zn | B. | CO2 | C. | Fe2O3 | D. | Ca(OH)2 |
18.黄铜(由锌和铜形成的合金)有较强的耐磨性能,在生活中有广泛的用途.三位同学为了测定黄铜屑样品组成,分三次取样品与稀硫酸反应,其实验数据记录如表:
请回答下列问题.
(1)根据质量守恒定律,可算出甲、乙、丙三位同学均生成0.2g氢气,通过对这三位同学的实验数据进行两两对比,可得出丙同学所取的稀硫酸与黄铜最可能符合恰好完全反应;
(2)假如该同学所取的稀硫酸与黄铜恰好完全反应,请求出:
①他所取的黄铜样品中锌的质量分数;
②所得溶液的溶质质量分数.(计算结果精确到0.1%)
| 甲 | 乙 | 丙 | |
| 样品质量/g | 25 | 30 | 25 |
| 稀硫酸质量/g | 120 | 80 | 80 |
| 充分反应后剩余物/g | 144.8 | 109.8 | 104.8 |
(1)根据质量守恒定律,可算出甲、乙、丙三位同学均生成0.2g氢气,通过对这三位同学的实验数据进行两两对比,可得出丙同学所取的稀硫酸与黄铜最可能符合恰好完全反应;
(2)假如该同学所取的稀硫酸与黄铜恰好完全反应,请求出:
①他所取的黄铜样品中锌的质量分数;
②所得溶液的溶质质量分数.(计算结果精确到0.1%)
