题目内容
4.加热10克氯酸钾和二氧化锰的混合物,反应后称得残留物的质量总和为9.52克,则生成氧气的质量为0.48 克;已知石蜡是蜡烛的主要成分,由蜡烛在空气中完全燃烧后的产物是CO2和H2O,判断石蜡中一定含有碳、氢两种元素,可能含有氧元素.分析 根据质量守恒定律,再利用反应前后固体质量差可以求出氧气的质量;根据质量守恒定律,在化学反应中,反应前后元素的种类没有改变;据此答题.
解答 解:
根据质量守恒定律,生成氧气的质量为:10g-9.52g=0.48g;
蜡烛燃烧时,由于空气提供了氧元素,且燃烧产物水和二氧化碳中含有碳、氢、氧三种元素,故可推断石蜡中一定含有碳、氢两种元素;可能含有氧元素;
答案:0.48g;碳、氢两种;氧.
点评 本题主要考查相关方面的计算,要注意遵循质量守恒定律;

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
19.沙特河拉伯森林中有一种吃铁鸟,它特别爱吃铁,经解剖发现,这种鸟的胃液里盐酸含量特别高,吃铁后发生反应:Fe+2HCl═FeCl2+H2↑.上述反应属于( )
| A. | 化合反应 | B. | 分解反应 | ||
| C. | 置换反应 | D. | 不属于上述三种反应类型 |
19.下列各组物质,在同一溶液中能大量共存的是( )
| A. | CaCl2和HCl | B. | FeCl3和NaOH | C. | MgSO4和NaOH | D. | AgNO3和CuCl2 |
9.现有下列七种物质:
①部分结冰的蒸馏水 ②铁水 ③稀有气体 ④过氧化氢 ⑤湖水 ⑥高锰酸钾加热制氧气后的剩余物 ⑦碘酒 ⑧液氮
其中肯定属于混合物的有(填序号,下同)③⑤⑥⑦,属于纯净物的有①②④⑧.
①部分结冰的蒸馏水 ②铁水 ③稀有气体 ④过氧化氢 ⑤湖水 ⑥高锰酸钾加热制氧气后的剩余物 ⑦碘酒 ⑧液氮
其中肯定属于混合物的有(填序号,下同)③⑤⑥⑦,属于纯净物的有①②④⑧.
16.下列化学方程式书写正确的是( )
| A. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$Hg+O2 | B. | KClO3$\frac{\underline{MnO_2}}{△}$KCl+O2↑ | ||
| C. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | D. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 |
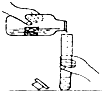 如图是小明同学倾倒液体的操作示意图,请指出三处不合理的地方
如图是小明同学倾倒液体的操作示意图,请指出三处不合理的地方