题目内容
4.天然气的主要成分是甲烷,甲烷是由碳元素和氢元素组成的最简单的有机化合物.已知甲烷中碳元素和氢元素的质量比为3:1,甲烷的相对分子质量为16,则甲烷的化学式为:CH4.分析 可以根据甲烷的相对分子质量和各种元素的质量比进行计算,从而求出化学式.
解答 解:甲烷中碳、氢两种元素的原子的相对原子质量之和分别为:
16×$\frac{3}{4}$=12;16×$\frac{1}{4}$=4;
即每个甲烷分子中含有的碳、氢的原子个数分别为:$\frac{12}{12}:\frac{4}{1}$=1;4;故化学式为:CH4.
点评 解答本题的关键是要掌握物质的元素组成和相关方面计算方法方面的知识,只有这样才能对问题做出正确的判断.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
15.一瓶CO和CO2的混合气体,己知碳元素和氧元素的质量比为5:8,则混台气体中CO和CO2的分子个数比为( )
| A. | 3:2 | B. | 4:1 | C. | 5:3 | D. | 2:1 |
12.下列方程式书写正确的是( )
| A. | CO2+Ca(OH)2=CaCO3+H2O | B. | Mg+O2=MgO2 | ||
| C. | 3Fe+2O2=Fe3O4 | D. | Fe+CuSO4=FeSO4+Cu |
13.2014年诺贝尔化学奖授予美国科学家埃里克•白兹格(Eric Betzig),德国科学家斯特凡•W•赫尔(Stefan W.Hell),美国科学家威廉姆•艾斯科•莫尔纳尔(William E.Moerner),以表彰他们在超分辨率荧光显微技术领域取得的成绩,将显微技术带入“纳米”领域.使运用激光谱技术观测化学反应时分子中原子的运动成为现实,你认为该技术不能观测到的是( )
| A. | 氮分子的不规则运动 | |
| B. | 氮原子结合成氮分子的过程 | |
| C. | 氮分子分解成氧原子的过程 | |
| D. | 氮原子内部的质子、中子、电子的运动 |
14.有一份铁粉与铜粉混合物的样品,为了解其组成,某同学进行了如下实验,所得数据如下:
(1)其中,酸过量的是第第二次;
(2)计算金属混合物中铁的质量分数.
(3)本实验所用的200g稀硫酸中含H2SO4多少克?
| 实验 | 第一次 | 第二次 | 第三次 |
| 取用金属混合物的质量/g | 20 | 20 | 40 |
| 取用稀硫酸的质量/g | 200 | 250 | 200 |
| 金属混合物与稀硫酸反应后过滤得到的干燥固体的质量/g | 4 | 4 | 24 |
(2)计算金属混合物中铁的质量分数.
(3)本实验所用的200g稀硫酸中含H2SO4多少克?
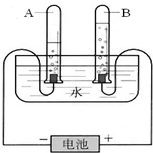 根据如图回答下列问题.
根据如图回答下列问题.