题目内容
建立宏观、微观和符号之间联系是学习化学的一种方法.
(1)在汞、水、氯化钠三种物质中,由离子构成的物质是 .
(2)属于单质的是 .属于氧化物的是 .
(3)乙基雌烯醇是一种参赛运动员禁用的兴奋剂,其化学式为C20H32O.乙基雌烯醇由 种元素组成,分子中H、O两种元素的质量比为 .
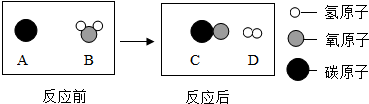
(4)已知:A和B在高温条件下生成C和D,各物质微观示意图如图所示:
下列说法正确的是 (填数字序号).
A.该反应中元素化合价都不变
B.化学变化中分子和原子均可再分
C.4种物质中属于氧化物的是B和C
D.若反应后生成1.8gD,则生成C的质量为8.4g
E.B与C物质的化学性质不同,是因为分子构成不同.
(1)在汞、水、氯化钠三种物质中,由离子构成的物质是
(2)属于单质的是
(3)乙基雌烯醇是一种参赛运动员禁用的兴奋剂,其化学式为C20H32O.乙基雌烯醇由
(4)已知:A和B在高温条件下生成C和D,各物质微观示意图如图所示:
| A | B | C | D |  表示碳原子表示氧原子表示氢原子 |
 |  |  |  |
A.该反应中元素化合价都不变
B.化学变化中分子和原子均可再分
C.4种物质中属于氧化物的是B和C
D.若反应后生成1.8gD,则生成C的质量为8.4g
E.B与C物质的化学性质不同,是因为分子构成不同.
考点:分子、原子、离子、元素与物质之间的关系,从组成上识别氧化物,单质和化合物的判别,微粒观点及模型图的应用,化学式的书写及意义,有关元素化合价的计算,元素质量比的计算,化学反应的实质
专题:化学反应模拟图型,物质的微观构成与物质的宏观组成,物质的分类
分析:(1)金属由原子直接构成,非金属氧化物由分子构成,盐类物质一般由离子构成;
(2)由同种元素组成的纯净物是单质,由两种元素组成,其中一种元素是氧元素的化合物物是氧化物解答;
(3)根据乙基雌烯醇化学式的含义进行分析解答;
(4)将图示以及符号意义转化为更直观的化学反应,从而结合反应进行方程式的进行分析与判断.从图示可知,A、B、C、D分别是CH4、H2O、CO、H2,该反应的化学方程式是:CH4+H2O
CO+3H2,据此分析解决即可.
(2)由同种元素组成的纯净物是单质,由两种元素组成,其中一种元素是氧元素的化合物物是氧化物解答;
(3)根据乙基雌烯醇化学式的含义进行分析解答;
(4)将图示以及符号意义转化为更直观的化学反应,从而结合反应进行方程式的进行分析与判断.从图示可知,A、B、C、D分别是CH4、H2O、CO、H2,该反应的化学方程式是:CH4+H2O
| ||
解答:解:
(1)构成物质的微粒有分子、原子和离子,金属汞是由汞原子构成的,水是由二氧化碳分子构成的,氯化钠是由钠离子和氯离子构成的.
(2)汞是由同种元素组成的纯净物是单质,水是由两种元素组成,其中一种元素是氧元素的化合物物是氧化物;
(3)由乙基雌烯醇的化学式可知,乙基雌烯醇是由碳、氢、氧三种元素组成的,1个乙基雌烯醇分子是由20个碳原子、32个氢原子和1个氧原子构成的,则乙基雌烯醇中氢元素与氧元素的原子个数比为(32×1):1=32:1.
(4)
由化学反应的微观示意图可知,A、B、C、D分别是CH4、H2O、CO、H2,该反应的化学方程式是:CH4+H2O
CO+3H2,由此可知:
A、由上述反应可知,氢元素的化合价由+1变为0,故错;
B、由微粒的变化可知,在反应前后原子的种类没有改变、分子的种类发生了改变,故错;
C、B、C分别是、H2O、CO,是由两种元素组成,其中一种元素是氧元素的化合物物是氧化物,故对;
D、根据CH4+H2O
CO+3H2,由此
28 6
x 1.8g
=
x=8.4g,故对;
E、分子可以保持物质的化学性质,B与C物质的化学性质不同,是因为分子构成不同,故对;
答案:
(1)氯化钠;
(2)汞;水;
(3)三;32:1
(4)AB
(1)构成物质的微粒有分子、原子和离子,金属汞是由汞原子构成的,水是由二氧化碳分子构成的,氯化钠是由钠离子和氯离子构成的.
(2)汞是由同种元素组成的纯净物是单质,水是由两种元素组成,其中一种元素是氧元素的化合物物是氧化物;
(3)由乙基雌烯醇的化学式可知,乙基雌烯醇是由碳、氢、氧三种元素组成的,1个乙基雌烯醇分子是由20个碳原子、32个氢原子和1个氧原子构成的,则乙基雌烯醇中氢元素与氧元素的原子个数比为(32×1):1=32:1.
(4)
由化学反应的微观示意图可知,A、B、C、D分别是CH4、H2O、CO、H2,该反应的化学方程式是:CH4+H2O
| ||
A、由上述反应可知,氢元素的化合价由+1变为0,故错;
B、由微粒的变化可知,在反应前后原子的种类没有改变、分子的种类发生了改变,故错;
C、B、C分别是、H2O、CO,是由两种元素组成,其中一种元素是氧元素的化合物物是氧化物,故对;
D、根据CH4+H2O
| ||
28 6
x 1.8g
| 28 |
| x |
| 6 |
| 1.8g |
x=8.4g,故对;
E、分子可以保持物质的化学性质,B与C物质的化学性质不同,是因为分子构成不同,故对;
答案:
(1)氯化钠;
(2)汞;水;
(3)三;32:1
(4)AB
点评:本题难度不大,主要考查了构成物质的微观粒子方面、化学式的知识,掌握常见物质的粒子构成、化学式的含义是正确解答本题的关键.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
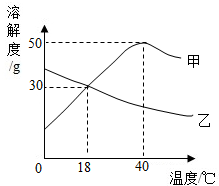 甲、乙两种固体物质的溶解度曲线如图所示,根据图中的信息判断,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,根据图中的信息判断,下列说法正确的是( )| A、甲的溶解度大于乙的溶解度 |
| B、降低温度可使甲、乙的饱和溶液变为不饱和溶液 |
| C、18℃时,甲、乙两种过饱和溶液的溶质质量分数相等 |
| D、物质甲的溶解度随温度的升高而升高 |
在反应M+2N═R+2Q中,3.2gM与N恰好完全反应后,生成8.8g的R,且反应生成的R和Q的质量比为11:9,则在此反应中N和Q的质量比是( )
| A、16:11 | B、16:9 |
| C、9:11 | D、4:9 |
学习化学时会遇到许多“相等”的关系,下列有关说法中正确的是( )
| A、化合物中元素化合价的正价与负价的数值一定相等 |
| B、参加化学反应的各物质的质量总和与反应后生成的各物质的质量总和一定相等 |
| C、溶液中阳离子个数与阴离子个数一定相等 |
| D、原子核内质子数与中子数一定相等 |
根据如图有关信息判断,下列说法正确的是( )


| A、镁离子(Mg2+)核内有12个质子 |
| B、镁的相对原子质量为24.31克 |
| C、在化学反应中,氯原子容易失去一个电子 |
| D、Mg2+和 Cl-最外层电子数不相等 |
推理是化学学习中常用的思维方法.下列推理不正确的是( )
| A、氯化钾溶液无色,说明高锰酸钾溶液呈紫红色与钾离子、水分子有关 |
| B、酸性溶液的pH小于7,氯化铵溶液是酸性溶液,所以氯化铵溶液的pH小于7 |
| C、碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性 |
| D、NaOH溶液中的OH-能与酸反应,则KOH溶液中的OH-也能与酸反应 |