题目内容
2.下列事实和解释相符的是( )| A. | 活性炭净水--活性炭能与水中杂质反应 | |
| B. | 盐酸清除铁锈--盐酸能与铁反应 | |
| C. | 汽油清洗油污--汽油起乳化作用 | |
| D. | 铜丝作导线--铜有良好的导电性 |
分析 A.根据活性炭的吸附性来分析;
B.根据稀盐酸的化学性质来分析;
C.根据汽油的作用来分析;
D.根据铜的导电性来分析.
解答 解:A.活性炭具有吸附作用,可以吸附水中的色素和异味,并不是与水中的杂质发生反应,错误;
B.铁锈的主要成分是氧化铁,能与盐酸反应生成氯化铁和水,故稀盐酸可以除铁锈,不是铁与盐酸反应,错误;
C.油污能溶解在汽油中,是溶解过程而不是乳化作用,错误;
D.铜具有良好的导电性,可用来制成导线,正确.
故选D.
点评 本题难度不大,掌握常见物质的性质以及物质的用途即可正确解答本题.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
12.从化学角度看,下了叙述不正确的是( )
| A. | 开发清洁新能源可以有效减少和防止酸雨的形成 | |
| B. | 常用钢丝球擦洗铝壶可以使其光亮洁净和更耐用 | |
| C. | 在铵态氮肥中加入熟石灰研磨可以闻到刺激性气味 | |
| D. | 合成纤维、合成橡胶等都是有机合成材料 |
11.碳在空气中燃烧可以生成CO或CO2,那么,氢气在空气中燃烧除生成水以外,能不能生成其他产物?某研究小组进行了如下探究:
【提出猜想】氢气在空气中燃烧可能生成过氧化氢
【查阅资料】①过氧化氢能使紫色酸性KMnO4溶液褪色;②锌粒与稀H2SO4反应制取氢气可能混有使酸性高锰酸钾溶液褪色的物质.
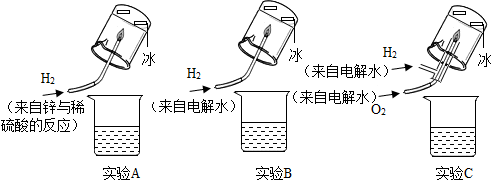
【设计并完成实验】小明设计了如图所示三套实验装置,点燃氢气并收集液体燃烧物.
小亮取4只试管,分别加入5滴酸性KMnO4溶液,再加入小明收集的液体产物和蒸馏水,测定恰好使紫色退去所需要的液体体积.
【得出结论】
(1)用锌与稀H2SO4反应制取氢气的化学方程式是Zn+H2SO4=ZnSO4+H2↑.
(2)实验④的实验目的是对照实验.
(3)由实验①、②、③的现象可知,氢气燃烧有(填“有”或“无”)过氧化氢生成.
(4)对比实验①和②可知,用锌粒与稀H2SO4反应制得氢气不纯(填“纯”或“不纯”).
(5)实验③比实验②更接近事实,因为它可排除空气中其他成分的干扰.
【反思与评价】
“用锌和稀H2SO4反应制氢气”与“电解水制氢气.氧气”,分别进行试验①和试验③,各自的优、缺点是:前者易于操作;后者反应物、生成物纯净(氢气、氧气和水),后者原子利用率高于前者(后者电解水产生的氢气和氧气恰好完全反应,而前者制氢气时产物还有硫酸锌,点燃时消耗空气中氧气).

【提出猜想】氢气在空气中燃烧可能生成过氧化氢
【查阅资料】①过氧化氢能使紫色酸性KMnO4溶液褪色;②锌粒与稀H2SO4反应制取氢气可能混有使酸性高锰酸钾溶液褪色的物质.
【设计并完成实验】小明设计了如图所示三套实验装置,点燃氢气并收集液体燃烧物.
小亮取4只试管,分别加入5滴酸性KMnO4溶液,再加入小明收集的液体产物和蒸馏水,测定恰好使紫色退去所需要的液体体积.
| 实验序号 | 加入液体 | 实验现象 |
| ① | 实验A 的收集液4.0mL | 褪色 |
| ② | 实验B 的收集液5.5mL | 褪色 |
| ③ | 实验C的收集液10.0mL | 不褪色 |
| ④ | 蒸馏水10.0mL | 不褪色 |
(1)用锌与稀H2SO4反应制取氢气的化学方程式是Zn+H2SO4=ZnSO4+H2↑.
(2)实验④的实验目的是对照实验.
(3)由实验①、②、③的现象可知,氢气燃烧有(填“有”或“无”)过氧化氢生成.
(4)对比实验①和②可知,用锌粒与稀H2SO4反应制得氢气不纯(填“纯”或“不纯”).
(5)实验③比实验②更接近事实,因为它可排除空气中其他成分的干扰.
【反思与评价】
“用锌和稀H2SO4反应制氢气”与“电解水制氢气.氧气”,分别进行试验①和试验③,各自的优、缺点是:前者易于操作;后者反应物、生成物纯净(氢气、氧气和水),后者原子利用率高于前者(后者电解水产生的氢气和氧气恰好完全反应,而前者制氢气时产物还有硫酸锌,点燃时消耗空气中氧气).
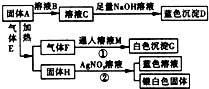 如图所示为各物质之间的转换关系,请回答下列问题:
如图所示为各物质之间的转换关系,请回答下列问题: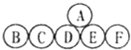 A、B、C、D、E、F分别是氧化铁、二氧化碳、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液中的一种:
A、B、C、D、E、F分别是氧化铁、二氧化碳、稀盐酸、氢氧化钙溶液、碳酸钠溶液、氢氧化钠溶液中的一种: