题目内容
14.下列关于Fe2O3的说法中,错误的是( )| A. | 该物质属于氧化物 | B. | 铁元素的化合价为+2价 | ||
| C. | 是铁锈的主要成分 | D. | 铁元素和氧元素的质量比为7:3 |
分析 根据化学式Fe2O3的组成、化合价、质量比进行判断解答即可.
解答 解:A、Fe2O3属于氧化物,正确;
B、铁元素的化合价为+3价,错误;
C、是铁锈的主要成分,正确;
D、铁元素和氧元素的质量比为=56×2:16×3=7:3,正确;
故先B
点评 本题难度不大,熟练掌握常见化学物质的化学式是正确解答此类题的关键.

练习册系列答案
相关题目
9.有NaHCO3和Na2CO3混合物13.7g,将其充分加热至固体质量不再减少,得剩余固体.将产生的气体通入足量的Ca(OH)2溶液中,产生5.0g沉淀.下列说法正确的是( )
| A. | 剩余固体为混合物 | |
| B. | 剩余固体的质量为11.5g | |
| C. | 原混合物中Na2CO3的质量大于NaHCO3 | |
| D. | 将剩余固体溶于足量的稀盐酸,产生4.4g CO2 |
5.下列从微观角度分析解释错误的是( )
| A. | 酒香不怕巷子深--分子总在不断的运动着 | |
| B. | 50ml酒精和50ml水相混合总体积小于100ml--分子之间有间隔 | |
| C. | 液态水变成水蒸气,体积增大--水分子的体积变大 | |
| D. | 氢气和液氢都可以做燃料--同种分子化学性质相同 |
2.在2N、N2、2CO、SO2中,数字“2”能用来表示分子个数的有( )
| A. | 1个 | B. | 2个 | C. | 4个 | D. | 5个 |
19.等物质的量的不同气体,相同的是( )
| A. | 体积 | B. | 分子个数 | C. | 质量 | D. | 原子个数 |
3.小聪同学家新换了水龙头,从说明书上了解到水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱.
【查阅资料】
(1)铬是银白色有金属光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
【结论与解释】
(1)小聪得出Fe、Cu、Cr三种金属的活动性由强到弱的顺序是Cr>Fe>Cu.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】
将铬片投入FeSO4溶液中,反应能(选填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
(3)配制农药波尔多液不能用铁制容器,用化学方程式解释Fe+CuSO4═FeSO4+Cu.
【查阅资料】
(1)铬是银白色有金属光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验操作 | 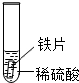 | 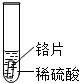 | 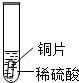 |
| 实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | 无明显现象发生(或无气泡生成,溶液也不变色) |
(1)小聪得出Fe、Cu、Cr三种金属的活动性由强到弱的顺序是Cr>Fe>Cu.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】
将铬片投入FeSO4溶液中,反应能(选填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
(3)配制农药波尔多液不能用铁制容器,用化学方程式解释Fe+CuSO4═FeSO4+Cu.
 工业上以石灰石和赤铁矿为主要原料可以制取B和G,其转化关系如图所
工业上以石灰石和赤铁矿为主要原料可以制取B和G,其转化关系如图所