题目内容
12.一包干燥的红色粉末可能含有Cu、Fe2O3、Fe(OH)3三种固体中的一种或两种组成.为确定其组成,请你参与探究.【提出猜想】红色粉末可能的组成有:
①只有Cu ②只有Fe2O3 ③只有Fe(OH)3④是Fe2O3与Fe(OH)3的混合物
⑤是Cu与Fe2O3的混合物 ⑥是Cu与Fe(OH)3的混合物
【资料获悉】
(1)2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O
(2)白色无水CuSO4遇水变蓝;
(3)Cu在FeCl3溶液中发生反应:2FeCl3+Cu=2FeCl2+CuCl2
探究思路】利用性质差异,先确定是否含Fe(OH)3、Cu等,逐步缩小范围,然后再选择
适当的试剂和方法探究其组成.(装置内空气中的水蒸气、CO2忽略不计)
【实验探究】
(1)甲同学取适量红色粉末装入试管中,按图1进行实验.结果无水CuSO4没有变蓝,从而排除猜想中的③④⑥(填猜想中的序号).

(2)在甲同学实验结论的基础上,乙同学另取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解,溶液变色.乙同学认为可以排除猜想中的①和⑤,而丙同学认为只能排除猜想①,你认为丙的观点正确(填“乙”或“丙”).
(3)为确定红色粉末的组成,丁同学提出提出两种方案:a通过A装置质量变化来计算,b通过B装置质量变化来计算.
【交流讨论】
(1)中先通CO气体的作用是排净装置中的空气(或防止CO和装置中的空气混合受热发生爆炸).
(2)选择a(填a或b)方案实验数据,计算确定红色粉末的组成更合理.
(3)A装置中发生反应的化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;实验中观察到A装置中的现象为部分红色粉末变黑.
【反思评价】戊同学指出:从环保角度,装置有严重不足之处.你认为该如何改进?在B装置后放一燃着的酒精灯将剩余气体烧掉.
【拓展延伸】有同学提出用H2代替CO,并将B装置换成盛有碱石灰(生石灰和氢氧化钠固体混合物)的干燥管也能确定其组成,你认为是否可行?可行(填“可行”或“不可行”).
分析 本题是一道综合性探究题,利用物质的性质不同设计实验加以甄别,来探究红色粉末的组成,先分别探究其中是否含有Fe(OH)3、Cu等,逐步缩小范围,然后再选择适当的试剂和方法通过实验探究确定其组成.
根据【资料获悉】中的(1)(2)(3)和探究(1)可排除猜想中的 ③④⑥,
根据【资料获悉】(3)和探究(2)可排除猜想中的①,故红色粉末可能是Fe2O3 或Cu、Fe2O3的混合物,探究(3)利用了一氧化碳的还原性和定量实验来确定是否有铜.
探究(3)要考虑到CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此,应先通CO排尽玻璃管中的空气,然后再加热.应考虑到CO有毒,排放到空气中会污染大气,显然,该装置没有对尾气进行处理.
在探究的同时也出现了与上述高考题中相同的防倒吸及尾气处理等考点.同时考查了一氧化碳还原氧化铁的实验操作要点实验现象等,对氢气的还原性也进行了衍生.
解答 解:【实验探究】
(1)根据资料 2Fe(OH)3 $\frac{\underline{\;加热\;}}{\;}$Fe2O3+3H2O,白色无水CuSO4遇水变蓝;加热红色粉末,结果无水CuSO4没有变蓝,从而排除猜想中的含有Fe(OH)3的选项③④⑥;故答案为:③④⑥;
(2)根据资料:Cu在FeCl3溶液中发生反应:2FeCl3+Cu=2FeCl2+CuCl2 ;取红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解,溶液变色,可推断排除猜想中的①,故红色粉末可能是Fe2O3 或Cu、Fe2O3的混合物;
所以说丙同学的观点正确;故答案为:丙;
【交流讨论】
(1)根据CO具有可燃性,与玻璃管中的空气混合受热会发生爆炸,因此,应先通CO排尽玻璃管中的空气,然后再加热.所以在装置A中先通CO气体的作用是:排净装置中的空气(或防止CO和装置中的空气混合受热发生爆炸);
故答案为:排净装置中的空气(或防止CO和装置中的空气混合受热发生爆炸);
(2)B装置,不能证明二氧化碳完全反应;应该选择A装置中实验数据计算来确定红色粉末的组成.故答案为:a;
(3)A装置中发生反应的化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;红色粉末是Cu、Fe2O3的混合物,因此实验中观察到A装置中的现象为:部分红色粉末变黑;
故答案为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;部分红色粉末变黑;
【反思评价】
此反应应考虑到CO有毒,排放到空气中会污染大气,显然,该装置没有对尾气进行处理;所以图装置有严重不足之处.改进方法为:在B装置后放一燃着的酒精灯将剩余气体烧掉(或用塑料袋等收集);
故答案为:在B装置后放一燃着的酒精灯将剩余气体烧掉(或用塑料袋等收集);
【拓展延伸】:CO还可以用H2代替,B装置换成盛有碱石灰(生石灰和氢氧化钠固体混合物)的干燥管,来确定该红色粉末的组成,可行;故答案为:可行.
((16分),各2分)(1)③④⑥; (2)丙
【交流讨论】(1)排净装置中的空气(或防止CO和装置中的空气混合受热发生爆炸);
(2)a; (3)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;部分红色粉末变黑;
【反思评价】在B装置后放一燃着的酒精灯将剩余气体烧掉(或用塑料袋等收集)
【拓展延伸】可行.
点评 此类题目主要对炼铁的实验原理、实验现象、操作步骤、尾气处理、装置连接及实验分析与评价等方面进行考查.熟练掌握该实验的反应原理以及实验注意事项是解决此类问题的关键.

 名校课堂系列答案
名校课堂系列答案| A. | MO | B. | MOH | C. | M2O3 | D. | M3O2 |
| A. | 加入适量的石灰石粉末 | B. | 加入适量的稀硫酸 | ||
| C. | 通入适量的二氧化碳气体 | D. | 加入适量的酸性废水 |
| A. | CO2 | B. | O2 | C. | SO2 | D. | HCl |
| A. | 实验室将废液直接倒入下水道 | |
| B. | 实验中未说明药品用量时,取用较多量药品进行实验 | |
| C. | 对废旧电池作深埋处理,消除其污染 | |
| D. | 化工生产中使原料尽可能地转化为产品 |
【知识回放】
金属活动性顺序:K Ca Na Mg Al ZnFeSn Pb(H)CuHg Ag Pt Au,请你
在横线上填写对应金属的元素符号.
【作出猜想】
猜想1.Cr>Fe>Cu;
猜想2.Fe>Cu>Cr;
猜想3.还有可能是Fe>Cr>Cu.
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的
同种稀硫酸.
【结论与解释】
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 |  |  |  |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | 无明显现象发生 |
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】
将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若不能进行,请说明理由;若能进行,请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
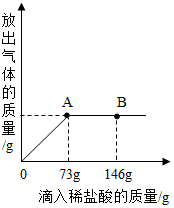 在一烧杯中盛有21.6g Na2CO3和NaCl组成的固体混合物,加足量水溶解,制成溶液.向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示:
在一烧杯中盛有21.6g Na2CO3和NaCl组成的固体混合物,加足量水溶解,制成溶液.向其中逐渐滴加溶质质量分数为10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示: