题目内容
为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液30g,逐滴加入氢氧化钡溶液40g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示).过滤后得滤渣2.33g.请你通过计算,求出氢氧化钡溶液的溶质质量分数.
反应方程式:H2SO4+Ba(OH)2=BaSO4↓+2H2O.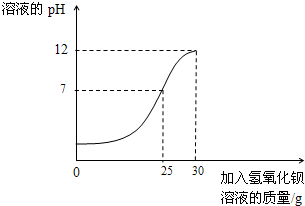
反应方程式:H2SO4+Ba(OH)2=BaSO4↓+2H2O.

由图象知当滴加的氢氧化钡溶液质量是25g时反应恰好完成,且沉淀的质量即是滤渣的质量2.33g,
设25g氢氧化钡溶液中氢氧化钡的质量为x
H2SO4+Ba(OH)2=BaSO4↓+2H2O
171 233
x 2.33g
=
x=1.71g 氢氧化钡溶液溶质质量分数为:
×100%=6.84%
答:氢氧化钡溶液的溶质质量分数为6.84%
设25g氢氧化钡溶液中氢氧化钡的质量为x
H2SO4+Ba(OH)2=BaSO4↓+2H2O
171 233
x 2.33g
| 171 |
| x |
| 233 |
| 2.33g |
x=1.71g 氢氧化钡溶液溶质质量分数为:
| 1.71g |
| 25g |
答:氢氧化钡溶液的溶质质量分数为6.84%

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
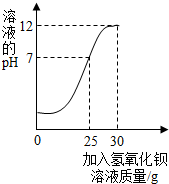 为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐滴加入氢氧化钡溶液30g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示).过滤后得滤液47.67g.请你通过计算,求出氢氧化钡溶液的溶质质量分数.可能用到的相对原子质量:H-1 O-16 S-32 Ba-137.
为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐滴加入氢氧化钡溶液30g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示).过滤后得滤液47.67g.请你通过计算,求出氢氧化钡溶液的溶质质量分数.可能用到的相对原子质量:H-1 O-16 S-32 Ba-137. (2012?闵行区二模)为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液15g,逐滴加入氢氧化钡溶液25g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示).过滤后得滤液37.67g.计算:
(2012?闵行区二模)为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液15g,逐滴加入氢氧化钡溶液25g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示).过滤后得滤液37.67g.计算: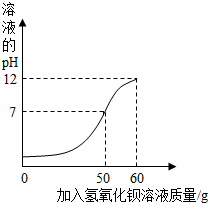 (2013?滨海县二模)为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液40g,逐滴加入氢氧化钡溶液60g,同时用pH计测定并记录反应过程中混合溶液pH变化情况如图.过滤后得滤液95.34g.已知:Ba(OH)2+H2SO4=Ba SO4↓+2H2O.请计算:
(2013?滨海县二模)为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液40g,逐滴加入氢氧化钡溶液60g,同时用pH计测定并记录反应过程中混合溶液pH变化情况如图.过滤后得滤液95.34g.已知:Ba(OH)2+H2SO4=Ba SO4↓+2H2O.请计算: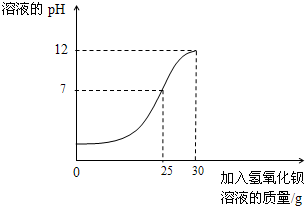 (2013?乐陵市三模)为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液30g,逐滴加入氢氧化钡溶液40g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示).过滤后得滤渣2.33g.请你通过计算,求出氢氧化钡溶液的溶质质量分数.
(2013?乐陵市三模)为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液30g,逐滴加入氢氧化钡溶液40g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示).过滤后得滤渣2.33g.请你通过计算,求出氢氧化钡溶液的溶质质量分数.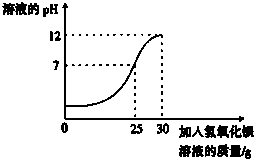 为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐渐加入氢氧化钡溶液30g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示),过滤后得滤液47.67g,请回答:
为测定某未知浓度的氢氧化钡溶液的溶质质量分数,取某稀硫酸溶液20g,逐渐加入氢氧化钡溶液30g,同时用pH计测定并记录反应过程中混合溶液pH变化情况(如图所示),过滤后得滤液47.67g,请回答: