题目内容
(1)请在下面的仪器中选择适当的仪器组成一套制取并收集干燥的氧气的装置,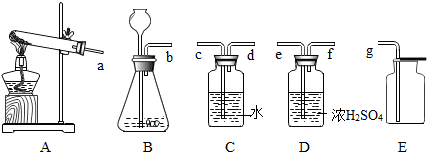
各仪器从左到右的接口顺序是 → → → (填各仪器接口处的字母).制取氧气的化学方程式为 .
(2)要测定生成的氧气的体积,必须选用除上图以外的仪器是 (填仪器名称)
(3)用B装置制取二氧化碳气体,反应的化学方程式为 .B装置中长颈漏斗伸入液面以下的目的是 ,收集二氧化碳的装置是 .
(4)查阅以下资料回答下列问题:
①制取氯气 (“可以“或者“不可以“)采用装置A,理由是 .
②制取氯气 (“可以”或者“不可以”)采用装置B,理由是 .

各仪器从左到右的接口顺序是
(2)要测定生成的氧气的体积,必须选用除上图以外的仪器是
(3)用B装置制取二氧化碳气体,反应的化学方程式为
(4)查阅以下资料回答下列问题:
①制取氯气
②制取氯气
考点:常用气体的发生装置和收集装置与选取方法,气体的干燥(除水),实验室制取氧气的反应原理,二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
氧气的密度比空气的密度大,不易溶于水;
氧气不能和浓硫酸反应,因此可以用浓硫酸干燥氧气;
(2)量筒可以用来测量液体的体积;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能够溶于水,密度比空气大;
(4)实验室通常利用二氧化锰和浓盐酸在加热条件下反应制取氯气.
氧气的密度比空气的密度大,不易溶于水;
氧气不能和浓硫酸反应,因此可以用浓硫酸干燥氧气;
(2)量筒可以用来测量液体的体积;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能够溶于水,密度比空气大;
(4)实验室通常利用二氧化锰和浓盐酸在加热条件下反应制取氯气.
解答:解:(1)各仪器从左到右的接口顺序是:通过B装置制取的氧气从b导管导出后,进入f导管,从e导管导出,进入g导管,即可收集到干燥的氧气;
制取氧气的化学方程式为:2H2O2
2H2O+O2↑.
故填:b;f;e;g;2H2O2
2H2O+O2↑.
(2)要测定生成的氧气的体积,必须选用除上图以外的仪器是量筒,因为量筒可以用来测量液体的体积.
故填:量筒.
(3)用B装置制取二氧化碳气体,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,B装置中长颈漏斗伸入液面以下的目的是防止二氧化碳从长颈漏斗逸出;
二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用E装置收集.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;防止二氧化碳从长颈漏斗逸出;E.
(4)①制取氯气不可以采用装置A,理由是因为制取氯气的药品是二氧化锰固体和浓盐酸.
故填:不可以;因为制取氯气的药品是二氧化锰固体和浓盐酸.
②制取氯气不可以采用装置B,理由是制取氯气需要加热.
故填:不可以;制取氯气需要加热.
制取氧气的化学方程式为:2H2O2
| ||
故填:b;f;e;g;2H2O2
| ||
(2)要测定生成的氧气的体积,必须选用除上图以外的仪器是量筒,因为量筒可以用来测量液体的体积.
故填:量筒.
(3)用B装置制取二氧化碳气体,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑,B装置中长颈漏斗伸入液面以下的目的是防止二氧化碳从长颈漏斗逸出;
二氧化碳能够溶于水,不能用排水法收集,密度比空气大,可以用向上排空气法收集,即用E装置收集.
故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;防止二氧化碳从长颈漏斗逸出;E.
(4)①制取氯气不可以采用装置A,理由是因为制取氯气的药品是二氧化锰固体和浓盐酸.
故填:不可以;因为制取氯气的药品是二氧化锰固体和浓盐酸.
②制取氯气不可以采用装置B,理由是制取氯气需要加热.
故填:不可以;制取氯气需要加热.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
下列各组物质按酸、碱、单质、氧化物顺序排列的是( )
| A、H2SO4 Na2O C CO |
| B、Mg(OH)2 CuSO4 C CO2 |
| C、C KOH HNO3 O2 SO3 |
| D、HCl NaOH O2 P2O5 |