题目内容
7.电解水的实验中,正极放出的是氧气,负极放出的是氢气,它们对应的体积比为1:2,这个反应的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,该实验的结果说明了水是由氢元素和氧元素组成;还验证了分子在化学变化中可分,原子不可分的结论.分析 根据电解水产生的氢气体积大,氧气体积小,正极产生氧气,负极产生氢气,电解水获得的实验结论,要记住.
解答 解:由正氧负氢,氢二氧一,可推出负极产生的是氢气,正极产生的是氧气,氢气和氧气的体积比为2:1,质量比根据方程式计算得1:8,通过电解水的实验可知,水是由氢元素和氧元素组成;在水分解的过程中水分子被分开成为氢氧两种原子,两种原子再重新组合成为氢氧两种分子,所以可知分子在化学变化中可分,原子不可分;该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
故答案为:氧气;氢气;1:2;2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;氢元素和氧元素;分子在化学变化中可分,原子不可分.
点评 要熟记正氧负氢,氢二氧一,电解水实验得到的结论有:水是由氢元素和氧元素组成,水是一种氧化物,说到物质用元素来解释,说到分子用原子来解释.

练习册系列答案
 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
18.家用衣领净的有效成分是NaClO,其中氯元素的化合价为( )
| A. | -1 | B. | +5 | C. | +3 | D. | +l |
16.在测定空气成分的实验中,下列做法与解释不合理的是( )
| A. | 先检查装置的气密性--保证实验能成功 | |
| B. | 用过量的红磷--保证把氧气充分消耗 | |
| C. | 冷却后再打开止水夹--使实验结果更准确 | |
| D. | 用红磷而不用木炭做--为了能看到产生的白烟 |
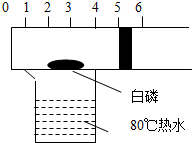 小明同学在学习完空气成分测定实验后改进了课本上的装置图如图(查阅资料得出白磷和红磷一样有可燃性,且燃烧后的生成物也相同,但白磷在40℃即可燃烧).回答下列问题:
小明同学在学习完空气成分测定实验后改进了课本上的装置图如图(查阅资料得出白磷和红磷一样有可燃性,且燃烧后的生成物也相同,但白磷在40℃即可燃烧).回答下列问题: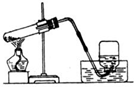 如图是实验室用高锰酸钾制氧气的装置图.指出图中的三处错误.
如图是实验室用高锰酸钾制氧气的装置图.指出图中的三处错误.