题目内容
13. 葡萄糖(C6H12O6)是生命活动中不可缺少的物质,如图是病人输液用的葡萄
葡萄糖(C6H12O6)是生命活动中不可缺少的物质,如图是病人输液用的葡萄糖注射液标签的部分内容.请回答:
(1)葡萄糖分子中碳、氢、氧原子个数比是1:2:1;葡萄糖中氧元素的质量分数是53.3%;
(2)该瓶注射液能给病人提供葡萄糖的质量是12.5 g;
在配制此浓度的葡萄糖溶液过程中,如果在用量筒量取水时仰视读数,则导致溶质质量分数< (填“>”或“<”或“=”)5%;
(3)某兴趣小组同学对某样品中葡萄糖的含量进行测定:取样品36g 于烧杯中,加入新制的氢氧化铜悬浊液后加热,实验完毕后称得生成砖红色沉淀的质量为1.44g.请计算该样品中葡萄糖的质量分数为多少?该产品是否合格?(C6H12O6+2Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$C6H12O7+Cu2O↓+2H2O ) (写出计算过程)
分析 根据物质的化学式可以判断组成元素的原子个数比,也可以计算组成元素的质量分数;
根据提供的数据可以计算葡萄糖的质量;
根据化学方程式和提供的数据可以计算葡萄糖的质量,进一步通过计算可以判断该产品是否合格.
解答 解:(1)葡萄糖分子中碳、氢、氧原子个数比是6:12:6=1:2:1;
葡萄糖中氧元素的质量分数为:$\frac{96}{180}$×100%=53.3%.
故填:1:2:1;53.3%.
(2)该瓶注射液能给病人提供葡萄糖的质量为:1g/cm3×250mL×5%=12.5g;
如果在用量筒量取水时仰视读数,会导致量取的水的体积偏高,则导致溶质质量分数<5%.
故填:12.5;<.
(3)设葡萄糖的质量为x,
C6H12O6+2Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$C6H12O7+Cu2O↓+2H2O,
180 144
x 1.44g
$\frac{180}{x}$=$\frac{144}{1.44g}$,
x=1.8g,
该样品中葡萄糖的质量分数为:$\frac{1.8g}{36g}$×100%=5%,
通过计算可知,该产品合格.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
4.物质的下列性质属于化学性质的是( )
| A. | 食盐易溶于水 | B. | 铝具有良好的延展性 | ||
| C. | 小苏打受热易分解 | D. | 食醋易挥发 |
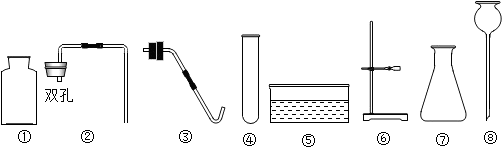
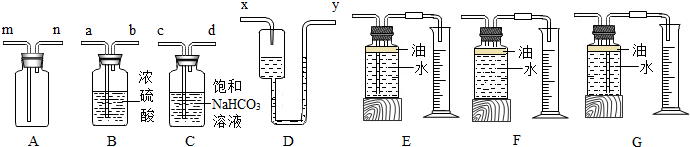
8.下列制取气体所用物质和装置均正确的是( )
| A. |  制取CO2 | B. |  制取氢气 | ||
| C. | 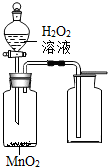 制取氧气 | D. |  制取氧气 |
18.以下是KCl的部分溶解度数据,下列说法中正确的是( )
| 温度/℃ | 0 | 20 | 40 | 60 |
| 溶解度/g | 27.6 | 34.0 | 40.0 | 45.5 |
| A. | KCl饱和溶液中不能再溶解其他物质 | |
| B. | 20℃时,100 g饱和KCl溶液中含KCl 34.0 g | |
| C. | 20℃时,KCl溶液中溶质的质量分数一定小于40℃时溶液中溶质的质量分数 | |
| D. | 60℃时将溶质质量分数为30%的KCl溶液降温至40℃时,有晶体析出 |
5. NaNO2是-种致癌物质.某兴趣小组为研究水中NaNO2的含量和消除污染的方法,进行如下目视比色法实验(比较溶液颜色深浅以测定物质浓度的方法),请你参与实验并填空:
NaNO2是-种致癌物质.某兴趣小组为研究水中NaNO2的含量和消除污染的方法,进行如下目视比色法实验(比较溶液颜色深浅以测定物质浓度的方法),请你参与实验并填空:
(1)测定方法的研究
配制质量分数为0.07%的NaNO2标准溶液,分别取0、2、4、6、8、10mL标准溶液于6支试管,加蒸馏水至总体积均为l0mL,分别加入约0.30gM粉未(M是氨基苯磺酸),振荡后制成颜色深浅不同的标准色阶.测定时取10mL水样,加入约0.30gM粉末,振荡后与标准色阶比较,得出颜色相同的色阶所含标准溶液的毫升数,再按稀释比例计算出水样中NaNO2的质量分数(水和稀溶液的密度均按l g•cm-3计算).
①配制质量分数为0.07%的NaNO2溶液l000mL,所需NaNO2的质量是0.7g;
②用上述方法测定某水样,其与含2mL标准溶液的色阶颜色相同,此水样中NaNO2的质量分数为0.014%;
(2)研究某水样在不同煮沸时间后NaNO2含量的变化
将另一水样用右图装置煮沸,测定不同煮沸时间NaNO2的质量分数,结果为:
①兴趣小组设计的右图实验装置用到了蒸气回流装置,其作用是保持水的总量不变;
②根据上述数据,可见此水样随煮沸时问的延长NaNO2的质量分数会逐渐增多;
(3)寻找能降低水中NaNO2含量的物质,研究消除污染的有效方法
查阅资料可知,加入醋酸或双氧水可降低水中NaNO2的质量分数,请设计实验证明少量醋酸是否有降低水中NaNO2质量分数的作用,填写下列实验报告:
 NaNO2是-种致癌物质.某兴趣小组为研究水中NaNO2的含量和消除污染的方法,进行如下目视比色法实验(比较溶液颜色深浅以测定物质浓度的方法),请你参与实验并填空:
NaNO2是-种致癌物质.某兴趣小组为研究水中NaNO2的含量和消除污染的方法,进行如下目视比色法实验(比较溶液颜色深浅以测定物质浓度的方法),请你参与实验并填空:(1)测定方法的研究
配制质量分数为0.07%的NaNO2标准溶液,分别取0、2、4、6、8、10mL标准溶液于6支试管,加蒸馏水至总体积均为l0mL,分别加入约0.30gM粉未(M是氨基苯磺酸),振荡后制成颜色深浅不同的标准色阶.测定时取10mL水样,加入约0.30gM粉末,振荡后与标准色阶比较,得出颜色相同的色阶所含标准溶液的毫升数,再按稀释比例计算出水样中NaNO2的质量分数(水和稀溶液的密度均按l g•cm-3计算).
①配制质量分数为0.07%的NaNO2溶液l000mL,所需NaNO2的质量是0.7g;
②用上述方法测定某水样,其与含2mL标准溶液的色阶颜色相同,此水样中NaNO2的质量分数为0.014%;
(2)研究某水样在不同煮沸时间后NaNO2含量的变化
将另一水样用右图装置煮沸,测定不同煮沸时间NaNO2的质量分数,结果为:
| 煮沸时间(小时) | 0 | 2 | 4 | 8 | 12 |
| NaNO2的质量分数 | 0 | 0 | 0.014% | 0.028% | 0.056% |
②根据上述数据,可见此水样随煮沸时问的延长NaNO2的质量分数会逐渐增多;
(3)寻找能降低水中NaNO2含量的物质,研究消除污染的有效方法
查阅资料可知,加入醋酸或双氧水可降低水中NaNO2的质量分数,请设计实验证明少量醋酸是否有降低水中NaNO2质量分数的作用,填写下列实验报告:
| 实验步骤 | 可能的实验现象 | 可能的结论 |
3.下列实验操作中,正确的是( )
| A. | 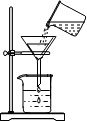 过滤 | B. | 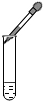 滴加液体 | C. |  熄灭酒精灯 | D. | 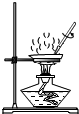 蒸发 |