题目内容
14.实验中学同学开展复分解反应研究性学习,设计了如下研究性学习思路:【练习质疑】下列各组物质间均能反应,写出③、④反应的化学方程式.
氢氧化钠溶液与盐酸 ②碳酸钠溶液与硫酸
③硫酸铜溶液和氢氧化钠溶液2NaOH+CuSO4=Na2SO4+Cu(OH)2↓.
④碳酸钠溶液和氯化钡溶液Na2CO3+BaCl2=BaCO3↓+2NaCl.
【研究讨论】上述反应为什么能够发生?是因为这些反应物中含有特殊的阴、阳离子,如①中有H+和OH-,②中有H+和CO32-,③中有Cu2+、OH-,④中有Ba2+、CO32-.
【构建网络】按照一定的顺序排列这些离子,就可以形成一种网络形式.在网络中,用短线相连的这些阴、阳离子能两两结合生成沉淀或气体或水.现有Ca2+、SO42-、NH4+,请将它们填入下面合适的“NH4+”中,使其形成一个更为完整的复分解反应网络.
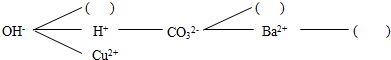
【拓展运用】通过形成的网络,可以判断化合物间能否共存,进行物质的鉴别,用于物质的除杂等.如硫酸钠溶液混有硫酸铵,可以加入NaOH(填写化学式)除去硫酸铵.
分析 运用酸碱盐的知识解决该题,根据复分解反应的条件生成沉淀或气体或生成水复分解反应才能发生填空,最后复分解反应网络用Ca2+、SO42-、NH4+的特性解决.
解答 解:
【练习质疑】硫酸铜溶液和氢氧化钠溶液反应生成氢氧化铜沉淀和硫酸钠,故③答案:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓;
碳酸钠溶液和氯化钡溶液反应生成碳酸钡和氯化钠,故④答案:Na2CO3+BaCl2=BaCO3↓+2 NaCl;
【研究讨论】阴、阳离子能两两结合生成沉淀或气体或水复分解反应就可发生,③中有Cu2+和OH-;④中有Ba2+和CO32-;
【构建网络】在这三种离子中NH4+与OH-能产生氨气和水,钡离子能与硫酸根离子产生白色沉淀,碳酸根离子与钙离子产生白色沉淀,故答案:NH4+;Ca2+;SO42-;
【拓展运用】除去硫酸钠中的硫酸铵实际是除去铵根离子,有题中复分解反应网络知选用碱,又不能引入新杂质所以选氢氧化钠,故答案:NaOH
答案:
【练习质疑】2NaOH+CuSO4=Na2SO4+Cu(OH)2↓;Na2CO3+BaCl2=BaCO3↓+2 NaCl;
【研究讨论】Cu2+、OH-; Ba2+、CO32-;
【构建网络】NH4+; Ca2+; SO42-;
【拓展运用】NaOH.
点评 本题在对复分解反应发生的条件分析的基础上对化学反应进行了考查并且延伸到物质鉴别,综合性强.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5. 铁路大提速后,为将短铁轨焊接成长铁轨,可在铁轨接口处加入氧化铁和铝粉的混合物,用镁条引燃发生反应,反应的化学方程式为:Fe2O3+2Al $\frac{\underline{\;点燃\;}}{\;}$ Al2O3+2Fe.有关该反应的下列说法中,该反应属于( )
铁路大提速后,为将短铁轨焊接成长铁轨,可在铁轨接口处加入氧化铁和铝粉的混合物,用镁条引燃发生反应,反应的化学方程式为:Fe2O3+2Al $\frac{\underline{\;点燃\;}}{\;}$ Al2O3+2Fe.有关该反应的下列说法中,该反应属于( )
 铁路大提速后,为将短铁轨焊接成长铁轨,可在铁轨接口处加入氧化铁和铝粉的混合物,用镁条引燃发生反应,反应的化学方程式为:Fe2O3+2Al $\frac{\underline{\;点燃\;}}{\;}$ Al2O3+2Fe.有关该反应的下列说法中,该反应属于( )
铁路大提速后,为将短铁轨焊接成长铁轨,可在铁轨接口处加入氧化铁和铝粉的混合物,用镁条引燃发生反应,反应的化学方程式为:Fe2O3+2Al $\frac{\underline{\;点燃\;}}{\;}$ Al2O3+2Fe.有关该反应的下列说法中,该反应属于( )| A. | 复分解反应 | B. | 分解反应 | C. | 化合反应 | D. | 置换反应 |
19.化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
【提出问题1】该氢氧化钠溶液是否变质了呢?
【实验探究1】
【提出问题2】该氢氧化钠溶液是全部变质还是部分变质呢?
【猜想与假设】猜想1:氢氧化钠溶液部分变质;猜想2:氢氧化钠溶液全部变质.
【查阅资料】①氯化钙溶液呈中性;②氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl.
【实验探究2】
【实验结论】该氢氧化钠溶液部分(填“部分”或“全部”)变质.
【反思与评价】
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:CO2+2NaOH=Na2CO3+H2O.
(2)在上述【实验探究2】中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案不可行(填“可行”或“不可行”).
【理解与应用】氢氧化钠溶液容易变质,必须密封保存.实验室必须密封保存的药品还有很多,试另举一例:澄清石灰水.
【提出问题1】该氢氧化钠溶液是否变质了呢?
【实验探究1】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量该溶液与试管中,向溶液中滴加盐酸,并不断振荡 | 有气泡冒出 | 氢氧化钠溶液一定变质了 |
【猜想与假设】猜想1:氢氧化钠溶液部分变质;猜想2:氢氧化钠溶液全部变质.
【查阅资料】①氯化钙溶液呈中性;②氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl.
【实验探究2】
| 实验步骤 | 实现现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡 | 有 白色沉淀生成 | 说明溶液中一定由碳酸钠 |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞试液 | 溶液变成红色 | 说明原溶液中一定有 氢氧化钠 |
【反思与评价】
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:CO2+2NaOH=Na2CO3+H2O.
(2)在上述【实验探究2】中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案不可行(填“可行”或“不可行”).
【理解与应用】氢氧化钠溶液容易变质,必须密封保存.实验室必须密封保存的药品还有很多,试另举一例:澄清石灰水.
4.二氧化硅可与氢氧化钠溶液反应生成硅酸钠与水.硅酸钠(Na2SiO3)中硅元素的化合价为( )
| A. | -4 | B. | ﹢2 | C. | ﹢4 | D. | ﹢5 |
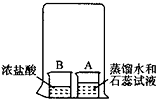 在烧杯A中装入20mL蒸馏水,滴入2~3滴石蕊试液;在烧杯B中装入10mL浓盐酸,然后用一只大烧杯把A、B两烧杯溶液罩在一起(如图所示).过几分钟后,可以观察到烧杯A中液体变成红色.请写出由该实验可知(浓)盐酸具有的一条性质:易挥发.
在烧杯A中装入20mL蒸馏水,滴入2~3滴石蕊试液;在烧杯B中装入10mL浓盐酸,然后用一只大烧杯把A、B两烧杯溶液罩在一起(如图所示).过几分钟后,可以观察到烧杯A中液体变成红色.请写出由该实验可知(浓)盐酸具有的一条性质:易挥发.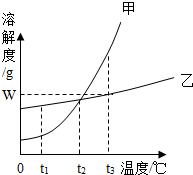 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线. (1)如图为电解水实验的装置图,CD试管之间产生气体的体积比约为2:1.
(1)如图为电解水实验的装置图,CD试管之间产生气体的体积比约为2:1.