题目内容
18.(1)某学习小组为测定M硫酸厂排放的废水中的硫酸含量进行如下实验:取50g废水于烧杯中,滴入质量分数为10%的氢氧化钠溶液(假定废水中其他成分不与氢氧化钠反应),当废水pH=时(填“>7”、“=7”、“<7”)反应恰好完全,测得消耗该氢氧化钠溶液8g,据此计算该废水中硫酸的质量分数.(2)M硫酸厂常用熟石灰对废水进行处理并产生硫酸钙,已知M厂每天用这种方法处理废水50吨,计算M厂每天理论上能产生多少吨硫酸钙.
分析 (1)根据硫酸的pH小于7,氢氧化钠溶液的pH值大于7,硫酸和氢氧化钠完全反应时,溶液的pH值等于,依据化学方程式进行计算;
(2)根据参加反应的硫酸的质量和化学方程式进行计算.
解答 解:(1)氢氧化钠和稀硫酸发生中和反应时,当废水pH=时反应恰好完全,
设废水中硫酸的质量分数为x
H2SO4+2NaOH=Na2SO4+2H20
98 80
50g×x 8g×10%
$\frac{98}{50g×x}$=$\frac{80}{8g×10%}$
x=1.96%
(2)设每天理论上能产生硫酸钙质量为y
H2SO4+Ca(OH)2=CaSO4+2H2O
98 136
1.96%×50t y
$\frac{98}{1.96%×50t}$=$\frac{136}{y}$
y=1.36t
故答案为:(1)=,废水中硫酸的质量分数为1.96%;
(2)每天理论上能产生硫酸钙质量为1.36t.
点评 本题主要考查有关含杂质物质的化学方程式计算和溶质质量分数的计算,难度较大.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
8.据报道,“毒淀粉”是在淀粉中添加了对人体有害的马来酸(C4H4O4),是无色晶体、能溶于水,下列说法正确的是( )
| A. | 马来酸属于氧化物 | |
| B. | 马来酸由三种元素组成 | |
| C. | 马来酸中碳元素的质量分数最大 | |
| D. | 10%的马来酸溶液中氧元素的质量分数约为5.52% |
6.下列叙述不正确的是( )
| A. | 在水的电解实验中与电源负极相连的导管中产生氢气 | |
| B. | 常用肥皂水检验硬水和软水 | |
| C. | 用5%的过氧化氢溶液制氧气,为加快该反应的速率常加少量二氧化锰作催化剂 | |
| D. | 用密度约为1.04g/cm3的6%的氯化钠溶液配制3%的氯化钠溶液一定要使用托盘天平 |
3.下列图示实验操作中,正确的是( )
| A. | 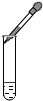 滴加液体 | B. | 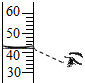 量筒读数 | C. | 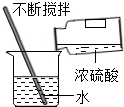 稀释浓硫酸 | D. | 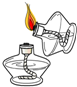 点燃酒精灯 |
10. 甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( )
甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( )
 甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( )
甲、乙两种固体的溶解度曲线如图所示.下列说法中,正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数 | |
| C. | 40℃时,分别在100 g水中加入40g 甲、乙,所得溶液溶质的质量分数相等 | |
| D. | 分别将甲和乙的饱和溶液从40℃降低到20℃,甲会析出晶体,乙则不会 |
9.下列物质的鉴别方法不可行的是( )
| A. | 用燃烧法鉴别棉线和羊毛线 | |
| B. | 用稀盐酸鉴别硫酸铵和硫酸钾 | |
| C. | 用石蕊溶液鉴别醋酸和硝酸钾溶液 | |
| D. | 用氯化钡溶液鉴别食盐水和碳酸钠溶液 |
10.要将一瓶接近饱和的石灰水变成饱和溶液,小明选择了如下方法.其中可行的是( )
①加入CaO ②加入Ca(OH)2③升高温度 ④降低温度.
①加入CaO ②加入Ca(OH)2③升高温度 ④降低温度.
| A. | ②③ | B. | ②④ | C. | ①②③ | D. | ①②④ |
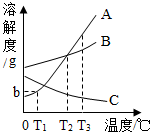 如图为A,B,C三种固体物质在水中的溶解度曲线,据此回答下列问题:
如图为A,B,C三种固体物质在水中的溶解度曲线,据此回答下列问题: