题目内容
11.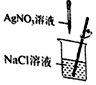 将10gNaC1溶液和10gAgNO3溶液混合,恰好完全反应.经过滤、洗涤、干燥、称量,得到2.87g沉淀.
将10gNaC1溶液和10gAgNO3溶液混合,恰好完全反应.经过滤、洗涤、干燥、称量,得到2.87g沉淀.(1)如图实验过程中,玻璃棒的作用是搅拌使反应快速、充分进行.
(2)计算反应后所得溶液中溶质的质量分数.(计算结果精确到0.1%)
分析 氯化钠和硝酸银反应生成白色沉淀氯化银和硝酸钠,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)如图实验过程中,玻璃棒的作用是搅拌使反应快速、充分进行.
故填:搅拌使反应快速、充分进行.
(2)设反应生成硝酸钠质量为x,
NaCl+AgNO3═AgCl↓+NaNO3,
143.5 85
2.87g x
$\frac{143.5}{2.87g}$=$\frac{85}{x}$,
x=1.7g,
反应后所得溶液中溶质的质量分数为:$\frac{1.7g}{10g+10g-2.87g}$×100%=9.9%,
答:反应后所得溶液中溶质的质量分数为9.9%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
1.2016年4月25日14时11分,尼泊尔(北纬28.2度,东经84.7度)发生8.1级地震,当地生产生活受到很大影响,尤其是饮用水的污染和短缺.下列几个步骤将河水转化为饮用水:①化学沉降(用明矾)②消毒杀菌(用漂白粉)③自然沉降④加热煮沸.以上处理过程最合理的顺序是( )
| A. | ③②①④ | B. | ③①②④ | C. | ③①④② | D. | ①③②④ |
6.如图是元素周期表的一部分,有关说法正确的是( )
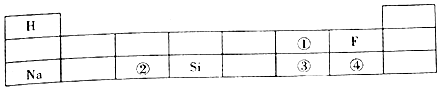

| A. | H既可表示氢元素,也可表示一个氢原子,还可表示氢气 | |
| B. | ①处元素和②处元素形成的常见化合物的化学式为Al2O3 | |
| C. | ③处元素为金属元素 | |
| D. | ④处元素的原子结构示意图为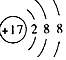 |
16.下列说法中正确的是( )
| A. | 有盐参加并生成的反应一定是复分解反应 | |
| B. | 氧气、水、高锰酸钾、酒精都含有氧元素,所以都属于氧化物 | |
| C. | 氢氧化镁属于碱类,所以能使酚酞变红 | |
| D. | 某固态物质的饱和溶液转化为不饱和溶液,溶质质量分数可能不变 |
20.下列说法正确的是( )
| A. | 煤炉上放一壶水可以防止CO中毒 | |
| B. | 过滤操作可以除去水中的所有杂质 | |
| C. | 生铁和钢的主要区别是含碳量不同 | |
| D. | 金刚石、石墨都是由碳原子构成的,所以都很坚硬 |

 化学让天更蓝.
化学让天更蓝.