题目内容
11.分析HCl、X、HClO、KClO3、KClO4的排布规律,X代表的是( )| A. | NaCl | B. | KClO | C. | Cl2 | D. | ClO2 |
分析 根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,分别计算HCl、HClO、HClO3、HClO4中氯元素的化合价,找出化合价排列规律;确定所给选项的四种物质中氯元素化合价,找出符合这一规律的物质.
解答 解:在化合物中正负化合价代数和为零,HCl、HClO、HClO3、HClO4中氯元素的化合价分别为-1、+1、+5、+7,可得出:物质是按氯元素化合价由低到高进行排列,则X中氯元素化合价应在-1和+1之间.
A、钠元素显+1价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x=0,则x=-1.
B、钾元素显+1价,氧元素显-2价,设氯元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+1)+y+(-2)=0,则y=+1.
C、单质中元素的化合价为0,因此氯气中氯元素化合价为0.
D、氧元素显-2价,设氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:z+(-2)×2=0,则z=+4.
C选项中氯元素化合价在-1和+1之间,符合要求.
故选C.
点评 本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法即可正确解答.

练习册系列答案
相关题目
6.目前我国对城市空气质量监测项目中,一般不考虑的是( )
| A. | 二氧化碳 | B. | 二氧化硫和一氧化碳 | ||
| C. | 二氧化氮 | D. | 可吸入颗粒物 |
3.下列说法正确的是( )
| A. | 溶液一定是液体 | |
| B. | 空气、合金也是溶液 | |
| C. | 40毫升酒精跟60毫升水混合一定得到100毫升溶液 | |
| D. | 盐水是溶液,糖水是溶液,两者混在一起,既有糖又有盐,则不是溶液了 |

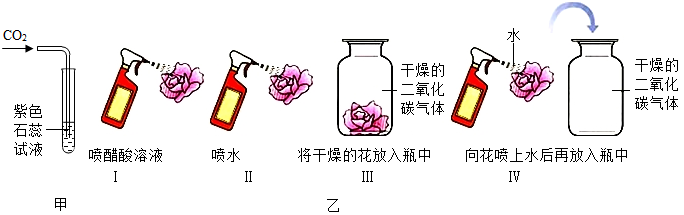
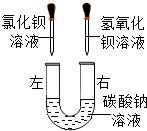 某化学活动小组在一次实验中进行了如图所示实验:
某化学活动小组在一次实验中进行了如图所示实验: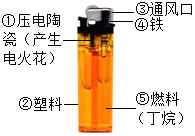 化学使人类生活更加丰富多彩,如打火机就给人们生活带来了方便.根据如图回答:
化学使人类生活更加丰富多彩,如打火机就给人们生活带来了方便.根据如图回答: