题目内容
3.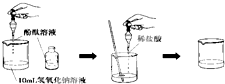 在烧杯中加入10ml氢氧化钠溶液,滴入几滴酚酞试液,再用滴管滴入稀盐酸,并不断搅拌,最终得到无色溶液.(如图所示)
在烧杯中加入10ml氢氧化钠溶液,滴入几滴酚酞试液,再用滴管滴入稀盐酸,并不断搅拌,最终得到无色溶液.(如图所示) (1)该过程中溶液的pH逐渐变小.
(2)酚酞的作用是指示反应何时恰好完全进行.
(3)该过程中发生反应的化学方程式是HCl+NaOH═NaCl+H2O.
分析 (1)根据氢氧化钠是一种常见的碱,其溶液呈碱性,能使无色酚酞变成红色,其溶液的酸碱度大于7;氢氧化钠能与盐酸发生中和反应,生成氯化钠和水,氯化钠溶液呈中性,因此在与盐酸恰好完全反应时,所得溶液呈中性,溶液的酸碱度等于7;继续滴加稀盐酸,由于盐酸的过量而使溶液酸性增强,溶液的酸碱度小于7解答;
(2)根据加酚酞的目的是指示酸碱何时完全反应解答;
(3)根据氢氧化钠能与盐酸发生中和反应,生成氯化钠和水解答.
解答 解:
(1)氢氧化钠是一种常见的碱,其溶液呈碱性,能使无色酚酞变成红色,其溶液的酸碱度大于7;氢氧化钠能与盐酸发生中和反应,生成氯化钠和水,氯化钠溶液呈中性,因此在与盐酸恰好完全反应时,所得溶液呈中性,溶液的酸碱度等于7;继续滴加稀盐酸,由于盐酸的过量而使溶液酸性增强,溶液的酸碱度小于7,酚酞仍为无色;
(2)加酚酞的目的是指示酸碱何时完全反应,故答案为指示反应何时恰好完全进行.
(3)氢氧化钠能与盐酸发生中和反应,生成氯化钠和水,反应的化学方程式是:HCl+NaOH═NaCl+H2O.
答案:
(1)小
(2)指示反应何时恰好完全进行
(3)HCl+NaOH═NaCl+H2O
点评 本题是考查中和反应过程中溶液pH的变化情况的,我们要知道向酸中加碱和向碱中加酸时,溶液pH的变化趋向.明确不同指示剂的变色范围.

练习册系列答案
相关题目
8.下列实验操作不能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中的CO | 在空气中点燃 |
| B | 区分羊毛与合成纤维 | 点燃,闻气味 |
| C | 分离铁粉和铜粉混合物 | 加入足量稀硫酸,过滤 |
| D | 区分NaOH和Ca(OH)2溶液 | 分别加入碳酸钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
 实验室制取甲烷可以用排水法收集,说明甲烷具有难溶于水的性质.
实验室制取甲烷可以用排水法收集,说明甲烷具有难溶于水的性质.