题目内容
实验表明浓硫酸可以盛装在铁制容器中(使铁发生钝化,不再反应),某地却报道盛装浓硫酸的铁桶在用水清洗时,遇明火却发生了爆炸,其原因是(化学方程式表示):
Fe+H2SO4═FeSO4+H2↑
Fe+H2SO4═FeSO4+H2↑
,2H2+O2
2H2O
| ||
2H2+O2
2H2O
.
| ||
分析:铁在常温下虽然不能够和浓硫酸反应,因此可以用铁桶盛装浓硫酸,但盛装过浓硫酸的铁桶用水清洗时,浓硫酸就变成了稀硫酸,铁就和稀硫酸反应生成了可燃性的氢气,若遇到明火就有可能会引起爆炸.
解答:解:盛装浓硫酸的铁桶在用水清洗时,浓硫酸被水稀释成稀硫酸,稀硫酸能与铁反应生成硫酸亚铁和氢气.
该反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑.生成的氢气与空气中的氧气在点燃条件下反应也可能发生爆炸,同时生成水.该反应的化学方程式为:2H2+O2
2H2O.因此清洗时应远离火源.
故答案为:Fe+H2SO4═FeSO4+H2↑;2H2+O2
2H2O;
该反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑.生成的氢气与空气中的氧气在点燃条件下反应也可能发生爆炸,同时生成水.该反应的化学方程式为:2H2+O2
| ||
故答案为:Fe+H2SO4═FeSO4+H2↑;2H2+O2
| ||
点评:本题难度不大,主要考查了硫酸的有关的化学性质及有关的化学方程式的书写,培养学生分析问题的能力;

练习册系列答案
相关题目
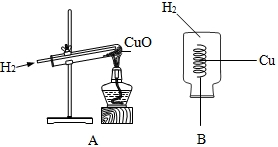
 (2005?绵阳)(1)硫酸亚铁是一种重要的化工原料,可用作杀虫剂、净水剂和木材防腐剂,还可用来治疗缺铁性贫血.工业上用废铁屑与稀硫酸反应制硫酸亚铁,主要反应的化学方程式为
(2005?绵阳)(1)硫酸亚铁是一种重要的化工原料,可用作杀虫剂、净水剂和木材防腐剂,还可用来治疗缺铁性贫血.工业上用废铁屑与稀硫酸反应制硫酸亚铁,主要反应的化学方程式为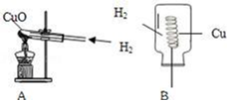
 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O 2CuO,CuO+H2SO4==CuSO4+2H2O
2CuO,CuO+H2SO4==CuSO4+2H2O
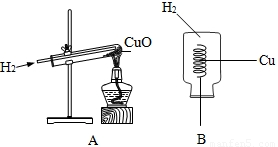
 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O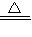 2CuO,CuO+H2SO4═CuSO4+2H2O
2CuO,CuO+H2SO4═CuSO4+2H2O