题目内容
4.某化学实验小组要检测黄铜(铜、锌合金)中金属铜的纯度,同学们取20g黄铜样品,向其中分三次共加入15g盐酸溶液,充分反应后测得实验结果如表:(Cu--64 H--1 Cl-35.5 Zn--65 )| 实验次数 | 1 | 2 | 3 |
| 盐酸质量 | 5g | 5g | 5g |
| 氢气质量 | 0.04g | m | 0.02g |
(1)第二次实验产生氢气的质量m0.04g.
(2)黄铜(铜、锌合金)中金属铜的纯度.
分析 (1)根据第一、三组中加入盐酸的量和生成的气体质量进行分析;
(2)根据生成氢气的量和锌与盐酸反应的方程式中的等量关系进行分析.
解答 解:(1)第一次加5克盐酸生成0.04克氢气,第三次加5克的盐酸还生成了0.02克的氢气,说明第二次反应中金属是过量的,也生成0.04克氢气,故答案为:0.04g;
(2)解:设共生成(0.04g+0.04g+0.02g=0.1g)氢气,需金属锌的质量为x.
Zn+2HCl=ZnCl2+H2↑
65 2
X 0.1g
$\frac{65}{X}$=$\frac{2}{0.1g}$
X=3.25g
合金中铜的质量分数即纯度:$\frac{20g-3.25g}{20g}$×100%=83.75%
答:黄铜(铜、锌合金)中金属铜的纯度为:83.75%.
点评 在解此类题时,首先分析题中考查的问题,然后结合表中的数据和反应的原理进行分析解答需要的数据,再进行进一步的计算.

练习册系列答案
相关题目
15.平时说的“菠菜中含有铁质”,其中所指的“铁”是( )
| A. | 铁原子 | B. | 单质铁 | C. | 铁元素 | D. | 铁分子 |
9.下列现象:①动物呼吸作用;②钢铁生锈;③白磷自燃;④火药爆炸,它们的共同点是( )
| A. | 都发光发热 | B. | 都是氧化反应 | C. | 都剧烈燃烧 | D. | 都有爆炸现象 |
16.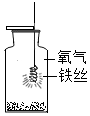 氧气是一种化学性质比较活泼的气体,关于铁丝在氧气中的反应叙述错误的是( )
氧气是一种化学性质比较活泼的气体,关于铁丝在氧气中的反应叙述错误的是( )
 氧气是一种化学性质比较活泼的气体,关于铁丝在氧气中的反应叙述错误的是( )
氧气是一种化学性质比较活泼的气体,关于铁丝在氧气中的反应叙述错误的是( )| A. | 生成物是一种黑色固体 | |
| B. | 生成物的质量大于参加反应的物质的质量总和 | |
| C. | 反应时出现火星四射,放热等现象 | |
| D. | 瓶底装少量水是防止热的生成物溅落造成集气瓶破裂 |
