题目内容
3.某药物牙膏包装盒上标明其中的抗腐蚀性药物的化学式为Na2FPO3,已知F为-1价 则在Na2FPO3中P元素化合价为( )| A. | +3 | B. | +4 | C. | +5 | D. | +6 |
分析 根据在化合物中正负化合价代数和为零,结合Na2FPO3的化学式进行解答即可.
解答 解:钠元素显+1价,F的化合价为-1,氧元素显-2价,设磷元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+(-1)+x+(-2)×3=0,则x=+5价.
故选:C.
点评 本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答此类题.

练习册系列答案
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
11.下列变化中,属于化学变化的是( )
| A. | 水制冰块 | B. | 菠萝榨汁 | C. | 食物腐烂 | D. | 氧气易溶于水中 |
8.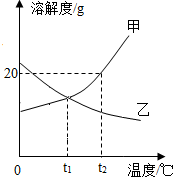 甲、乙两种物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种物质的溶解度曲线如图,下列说法中正确的是( )
 甲、乙两种物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种物质的溶解度曲线如图,下列说法中正确的是( )| A. | 升温能使甲物质的不饱和溶液变为饱和溶液 | |
| B. | t2℃时,乙物质的溶解度比甲物质的溶解度大 | |
| C. | t1℃时,甲、乙两种饱和溶液的溶质质量分数相同 | |
| D. | t2℃时将甲、乙两饱和溶液降温到t1℃时,乙析出晶体较多 |
12.正在生产的国产大型客机C919部分机身采用了铝锂合金,这种材料具有较高的强度和适宜的延展性.铝锂合金中铝(A1)元素与锂(Li)元素的本质区别是( )
| A. | 物质类别不同 | B. | 原子的质子数不同 | ||
| C. | 原子的电子数不同 | D. | 原子的质量不同 |
13.下图是某兴趣小组进行的四个实验操作,其中正确的是( )
| A. | 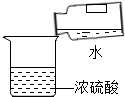 稀释浓硫酸 | B. | 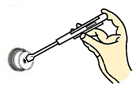 用测电笔判别零线或火线 | ||
| C. | 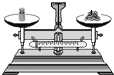 称量氯化钠 | D. | 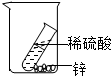 验证质量守恒定律 |
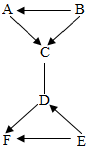 A、B、C、D、E、F都是我们已学过的物质,其中C是常用于光合作用和灭火的气体,常温下D是一种液体.它们之间的关系如图所示(图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系).
A、B、C、D、E、F都是我们已学过的物质,其中C是常用于光合作用和灭火的气体,常温下D是一种液体.它们之间的关系如图所示(图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系).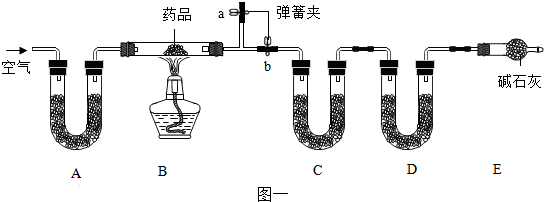

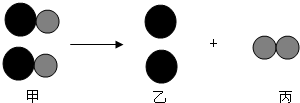
 ”和“
”和“ ”分别表示不同质子数的原子在化学变化前后的微观模拟示意图下.请回答下列问题:
”分别表示不同质子数的原子在化学变化前后的微观模拟示意图下.请回答下列问题: