题目内容
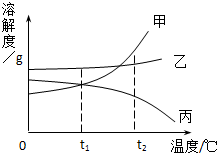 如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在),请根据图回答:
如图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线.现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在),请根据图回答:(1)t1℃时,三种物质溶解度的大小关系是
(2)t2℃时,将三种饱和溶液分别恒温蒸发相同质量的水,析出晶体最多的是
(3)将三种饱和溶液分别从t2℃降温到t1℃时,所得溶液中溶质的质量分数由大到小的顺序为
考点:固体溶解度曲线及其作用,晶体和结晶的概念与现象,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)据溶解度曲线可比较同一温度下不同物质的溶解度大小;
(2)据该温度下三种物质的溶解度分析解答;
(3)据 物质的溶解度随温度变化情况及饱和溶液中溶质的质量分数分析解答.
(2)据该温度下三种物质的溶解度分析解答;
(3)据 物质的溶解度随温度变化情况及饱和溶液中溶质的质量分数分析解答.
解答:解:(1)由图可知:t1℃时,三种物质溶解度的大小关系是乙>甲=丙;
(2)t2℃时三种物质的溶解度由大到小的顺序依次是甲、乙、丙,即等量的水中溶解的甲最多,所以将三种饱和溶液分别恒温蒸发相同质量的水,析出晶体最多的是甲;
(3)由图可知:甲的溶解度随温度降低而减小,乙的溶解度随温度变化不大,丙的溶解度随温度降低而增大;所以将三种饱和溶液分别从t2℃降温到t1℃时,甲、乙均析出晶体,丙的溶解度变大,变为不饱和溶液,溶质的质量分数与降温前相等;据饱和溶液中溶质的质量分数的计算式
×100%可知:溶解度大则溶质的质量分数大,t1℃时乙的溶解度大于甲的溶解度大于t2℃时丙的溶解度,故所得溶液中溶质的质量分数由大到小的顺序为乙>甲>丙;
故答案为:(1)乙>甲=丙;(2)甲;(3)乙>甲>丙.
(2)t2℃时三种物质的溶解度由大到小的顺序依次是甲、乙、丙,即等量的水中溶解的甲最多,所以将三种饱和溶液分别恒温蒸发相同质量的水,析出晶体最多的是甲;
(3)由图可知:甲的溶解度随温度降低而减小,乙的溶解度随温度变化不大,丙的溶解度随温度降低而增大;所以将三种饱和溶液分别从t2℃降温到t1℃时,甲、乙均析出晶体,丙的溶解度变大,变为不饱和溶液,溶质的质量分数与降温前相等;据饱和溶液中溶质的质量分数的计算式
| 溶解度 |
| 溶解度+100g |
故答案为:(1)乙>甲=丙;(2)甲;(3)乙>甲>丙.
点评:了解溶解度概念的含义、溶解度曲线的意义及其应用,饱和溶液中溶质的质量分数的计算方法,才能结合题意灵活分析解答.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
下列各组元素的原子结构示意图中,具有相似化学性质的一组元素是( )
A、 |
B、 |
C、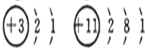 |
D、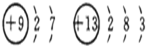 |
目前,很多不法商贩使用“西瓜膨大增甜剂”使西瓜迅速膨大并且增甜,而这种药剂的名称叫氯吡苯脲,化学式为C12H10ClN3O,下列关于氯吡苯脲的认识正确的是( )
| A、氯吡苯脲由5种元素组成 |
| B、氯吡苯脲中元素的质量比为12:10:1:3:1 |
| C、其相对分子质量为609.5g |
| D、它是一种氧化物 |
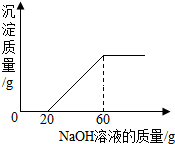 某混合溶液中含有氯化铜和稀盐酸,向其中慢慢滴入20%的氢氧化钠溶液并振荡,所加氢氧化钠溶液的质量与生成沉淀的质量的关系如图所示:
某混合溶液中含有氯化铜和稀盐酸,向其中慢慢滴入20%的氢氧化钠溶液并振荡,所加氢氧化钠溶液的质量与生成沉淀的质量的关系如图所示: