题目内容
请根据以下三个实验回答问题:

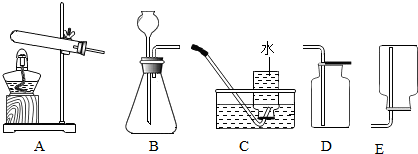
(1)A实验:玻璃管①中产生的气体是 ;反应方程式为 .
(2)B实验:如果实验数据小于21%,可能原因是
(3)C中实验现象是:①小烧杯中有大量气泡产生,② .其中现象①中发生化学反应的方程式是 .该实验说明二氧化碳具有的性质是 、 .

(1)A实验:玻璃管①中产生的气体是
(2)B实验:如果实验数据小于21%,可能原因是
(3)C中实验现象是:①小烧杯中有大量气泡产生,②
考点:电解水实验,空气组成的测定,二氧化碳的物理性质,二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:(1)根据电解水实验的现象和结论分析回答;
(2)根据测定空气中氧气含量试验的注意事项分析回答;
(3)根据二氧化碳的性质分析回答.
(2)根据测定空气中氧气含量试验的注意事项分析回答;
(3)根据二氧化碳的性质分析回答.
解答:解:(1)由装置可知,A实验是电解水,玻璃管①中产生的气体较少是氧气;反应方程式为2H2O
2H2↑+O2↑.
(2)由装置可知,B实验是测定空气中氧气含量的实验,如果实验数据小于21%,可能原因是:铜的量太少,氧气没完全反应,装置漏气等;
(3)由于盐酸与碳酸钠反应生成了氯化钠、二氧化碳和水,所以,C中实验现象是:①小烧杯中有大量气泡产生,②下面的蜡烛先熄灭,上面的蜡烛后熄灭.其中现象①中发生化学反应的方程式是:Na2CO3+2HCl═2NaCl+H2O+CO2↑.该实验说明二氧化碳具有的性质是不能燃烧,不支持燃烧、密度比空气大.
故答为:(1)氧气,2H2O
2H2↑+O2↑;(2)铜的量太少,氧气没完全反应,装置漏气等;(3)下面的蜡烛先熄灭,上面的蜡烛后熄灭,Na2CO3+2HCl═2NaCl+H2O+CO2↑;不能燃烧,不支持燃烧、密度比空气.
| ||
(2)由装置可知,B实验是测定空气中氧气含量的实验,如果实验数据小于21%,可能原因是:铜的量太少,氧气没完全反应,装置漏气等;
(3)由于盐酸与碳酸钠反应生成了氯化钠、二氧化碳和水,所以,C中实验现象是:①小烧杯中有大量气泡产生,②下面的蜡烛先熄灭,上面的蜡烛后熄灭.其中现象①中发生化学反应的方程式是:Na2CO3+2HCl═2NaCl+H2O+CO2↑.该实验说明二氧化碳具有的性质是不能燃烧,不支持燃烧、密度比空气大.
故答为:(1)氧气,2H2O
| ||
点评:本题所涉及的三个实验都是课本题中的重要的实验,加强实验的学习,提高实验的能力,是解答本类题的基础.

练习册系列答案
相关题目
用于检验二氧化碳气体的物质是( )
| A、水 | B、燃着的木条 |
| C、澄清石灰水 | D、带火星的木条 |
将含有BaCl2和两种固体的混合物,溶于水得白色沉淀,过滤向滤液中滴加AgNO3溶液产生白色沉淀,加入稀硝酸沉淀不溶解,根据这些现象判断下列说法中不正确的是( )
| A、混合物溶于水后过滤,滤液中可能含有Na2CO3 |
| B、向滤液中加入AgNO3溶液所产生的白色沉淀是AgCl |
| C、混合物溶于水时所得白色沉淀是BaCO3 |
| D、混合物溶于水后过滤,滤液中肯定不含Na2CO3 |
如图实验过程中,下列说法错误的是( )
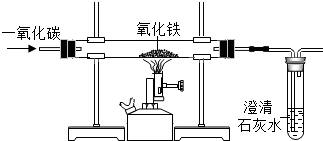

| A、实验现象:红色粉末变成黑色,澄清石灰水变浑浊 | ||||
| B、实验操作:加热前,应先通一会儿一氧化碳,以防爆炸 | ||||
C、实验原理:CO+FeO
| ||||
| D、实验反思:为了减少空气污染,应增加尾气处理装置 |
下列化学符号中数字“2”表示的意义正确的是( )
| A、Ca2+:表示钙元素的化合价为+2价 |
| B、2CO:表示二个一氧化碳分子 |
| C、CO2:表示一个二氧化碳分子中含有一个氧分子 |
| D、Mg2+:表示每个镁离子带两个单位正电荷 |