题目内容
12. 化学小组用一定量的AgNO3和Cu(NO3)2混合溶液进行了如图实验,当溶液甲恰好呈浅绿色,需向混合溶液加入适量的铁;溶液甲中一定含有的溶质是Cu(NO3)2、Fe(NO3)2(写化学式),请写出该实验过程中的方程式Fe+2AgNO3=Fe(NO3)2+2Ag(写出一个即可)
化学小组用一定量的AgNO3和Cu(NO3)2混合溶液进行了如图实验,当溶液甲恰好呈浅绿色,需向混合溶液加入适量的铁;溶液甲中一定含有的溶质是Cu(NO3)2、Fe(NO3)2(写化学式),请写出该实验过程中的方程式Fe+2AgNO3=Fe(NO3)2+2Ag(写出一个即可)
分析 根据亚铁离子在溶液中显浅绿色,铁会与硝酸银、硝酸铜反应生成硝酸亚铁和铜、银进行分析.
解答 解:亚铁离子在溶液中显浅绿色,当溶液甲恰好呈浅绿色,需向混合溶液加入适量的铁,铁会与硝酸银、硝酸铜反应生成硝酸亚铁和铜、银,只要硝酸亚铁的量大于硝酸铜的量,溶液就显浅绿色,所以刚好是浅绿色的时候铜不可能全部被置换出来,所以溶液甲中一定含有的溶质是Cu(NO3)2、Fe(NO3)2;铁和硝酸银反应生成硝酸亚铁和银,化学方程式为:Fe+2AgNO3=Fe(NO3)2+2Ag.
故答案为:铁,Cu(NO3)2、Fe(NO3)2;Fe+2AgNO3=Fe(NO3)2+2Ag.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序的意义结合题目的信息分析滤液和滤渣的成分.

练习册系列答案
相关题目
6.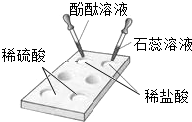 对于如图所示的实验下列说法不正确的是( )
对于如图所示的实验下列说法不正确的是( )
 对于如图所示的实验下列说法不正确的是( )
对于如图所示的实验下列说法不正确的是( )| A. | 该实验仪器的名称叫点滴板,使用该仪器最大的优点是节约药品 | |
| B. | 石蕊遇盐酸变红,酚酞遇盐酸不变色,因此可以利用酸碱指示剂检测溶液的酸碱度 | |
| C. | 稀硫酸和稀盐酸一样也能使石蕊和酚酞发生相同的颜色变化,因其溶液中都含H+ | |
| D. | 可以利用石蕊试液区分盐酸、氯化钠溶液和氢氧化钠溶液 |
1.下列变化中,属于物理变化的是( )
| A. | 酒精燃烧 | B. | 牛奶变质 | C. | 钢铁生锈 | D. | 石块粉碎 |
17.向无色溶液中加入氯化钡溶液后有白色沉淀生成,则该溶液一定是( )
| A. | 硝酸银 | B. | 硫酸钠 | ||
| C. | 硝酸银和硫酸钠的混合物 | D. | 不能确定 |
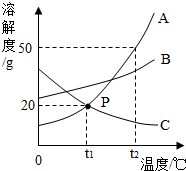 根据如图A、B、C三种固体的溶解度曲线回答;
根据如图A、B、C三种固体的溶解度曲线回答;