题目内容
6.某校化学兴趣小组就空气中氧气的含量进行实验探究:
(1)小组同学设计了如图1所示的两套装置,你认为合理的是A(填字母)为了确保实验的成功,在装药品之前应该检查装置的气密性.
(2)红磷在集气瓶中发生反应的文字表达式为磷+氧气$\stackrel{点燃}{→}$五氧化二磷.该实验中红磷稍过量,目的是充分消耗瓶内氧气
(3)小组同学做完实验后发现水进入集气瓶的量远少于理论值.经讨论,同学们认为造成该现象的原因可能有红磷不足或未冷却打开止水夹.
(4)若将红磷换成炭粉,该实验能否获得成功?不能,理由是产生新的气体二氧化碳.
(5)小淳同学对实验装置进行了大胆的改造,设计了如图2的装置.请根据图示回答下列问题:
①闭合电源开关,可以观察到白磷剧烈燃烧,产生大量白烟.
②装置冷却到室温时,可观察到U型管内左侧液面上升到刻度“1”处.
③通过这个实验得出的结论是空气中氧气约占1/5体积
④此实验还可推知反应后剩余气体的两点性质是:无色、难溶于水、不燃烧也不支持燃烧.
分析 (1)根据为保证红磷与空气中的氧气充分反应,必须把红磷放在集气瓶的中下部;检验装置的气密性是为了确保准确测空气组成,减少误差进行分析;
(2)根据红磷和氧气在点燃的条件下生成五氧化二磷进行分析;
(3)根据水进入集气瓶的量远少于理论值,说明集气瓶内的氧气没有消耗完或者外界的空气进入集气瓶内等原因进行分析;
(4)根据木炭和氧气反应会生成二氧化碳气体,二氧化碳气体也能产生压强进行分析;
(5)根据用白磷测定空气组成的实验原理、操作、现象、结论和注意事项,分析解答本题.
解答 解:(1)保证集气瓶中的氧气与红磷完全反应,故选A;
为了保证实验能够成功,实验前应该检查装置的气密性,确保成功测定空气主要组成成分;
(2)红磷和氧气在点燃的条件下生成五氧化二磷,文字表达式为:磷+氧气$\stackrel{点燃}{→}$五氧化二磷,该实验中红磷稍过量,目的是:充分消耗瓶内氧气;
故答案为:(1)A,检查装置的气密性;
(3)水进入集气瓶的量远少于理论值,说明集气瓶内的氧气没有消耗完或者外界的空气进入集气瓶内等原因,所以认为造成该现象的原因可能有:红磷不足或未冷却打开止水夹或气密性不良;
(4)木炭和氧气反应会生成二氧化碳气体,二氧化碳气体也能产生压强,所以不能将红磷换成炭粉,理由是:产生新的气体二氧化碳;
(5)①闭合电源开关,电热丝发热,当达到白磷的燃点时,白磷燃烧,产生白烟;
②装置冷却到室温时,可观察到U型管内左侧液面上升到刻度1处;
③通过这个实验得出的结论是:氧气约占空气体积的五分之一;
④此实验还可推知反应后剩余气体的性质有:不溶于水也不支持燃烧.
(2)磷+氧气$\stackrel{点燃}{→}$五氧化二磷,充分消耗瓶内氧气;
(3)红磷不足或未冷却打开止水夹或气密性不良;
(4)不能,产生新的气体二氧化碳;
(5)①剧烈燃烧,产生大量白烟;
②上升到刻度“1”处;
③空气中氧气约占1/5体积;
④无色、难溶于水,不燃烧也不支持燃烧.
点评 本题主要考查用白磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大,需学生结合课本知识仔细推敲.

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案| A. | 碳+氧气$\stackrel{点燃}{→}$二氧化碳 | B. | 酒精+氧气$\stackrel{点燃}{→}$二氧化碳+水 | ||
| C. | 氧化汞$\stackrel{加热}{→}$汞+氧气 | D. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 |
| A. | 禁止污水直接排放到河流中 | B. | 增加公园,扩大绿化面积 | ||
| C. | 将垃圾收集起来焚烧 | D. | 鼓励市民出行乘坐公交少开私家车 |
| A. | 天平称得某物质的质量为36.73g | |
| B. | 用100mL的量筒量取8mL酒精 | |
| C. | 给液体加热时,盛液量不能超过试管容积的$\frac{2}{3}$ | |
| D. | 给试管中固体加热时,试管口略向下倾斜 |
 ”、“
”、“ ”、“
”、“ ”,如图为三种物质之间发生化学反应前后的状况,则该反应的化学方程式中,A、B、C三物质的化学式前的系数之比为( )
”,如图为三种物质之间发生化学反应前后的状况,则该反应的化学方程式中,A、B、C三物质的化学式前的系数之比为( )
| A. | 3:1:2 | B. | 4:1:3 | C. | 4:1:2 | D. | 3:1:3 |
【猜想】
Ⅰ.氧化铁不是反应的催化剂、也不参与反应,质量和化学性质反应前后均不变;
Ⅱ.氧化铁参与反应产生氧气,反应前后质量不变,但化学性质发生了改变;
Ⅲ.氧化铁是反应的催化剂,反应前后质量和化学性质均不变.
【实验】用天平称0.2g氧化铁,用试管取5mL5%的过氧化氢溶液,进行如下实验:
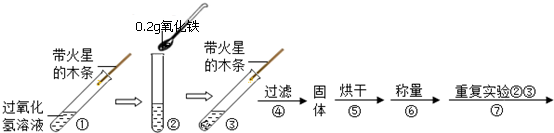
(注:氧化铁不溶于水,过滤可与水分离)
(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 带火星的木条复燃. | 质量不变 | 过氧化氢溶液中: 有气泡冒出 | 猜想Ⅰ、Ⅱ不成立; 猜想Ⅲ成立. |
(3)写出上述有关过氧化氢分解的文字表达式过氧化氢$\stackrel{氧化铁}{→}$水+氧气.
(4)步骤⑦重复实验②、③的目的是判断氧化铁在过氧化氢分解前后化学性质是否改变.
【继续探究】从上述实验得出氧化铁是反应的催化剂.对同种催化剂,有哪些因素可能影响催化效果?请提出猜想并设计实验进行探究.(注意:至少探究两种因素,答对一种因素奖励2分,本題最多奖励4分,化学试卷总分不超过60分)
 A,B两图分别表示硫、铁丝在氧气中燃烧的示意图,请回答:
A,B两图分别表示硫、铁丝在氧气中燃烧的示意图,请回答: