题目内容
1.工业上制备H2反应,其中用“●”表示氢原子,用“ ”代表氧原子,用“
”代表氧原子,用“ ”代表碳原子,
”代表碳原子,
(1)该反应共涉及4种分子.
(2)在该反应前后化合价发生变化有碳、氢元素.
(3)该所表示化学方程式为CH4+H2O $\frac{\underline{\;高温\;}}{\;}$CO+3H2.
分析 根据微粒的微观示意图,分析分子、原子的种类,从而书写出相应的化学方程式,由原子的种类得出元素的种类,根据单质中元素的化合价以及化合物中元素的化合价分析解答;
解答 解:(1)由微观图,反应前两分子构成不同,为两种物质的分子;反应后的四个分子中,其中三个分子都是由2个相同的原子构成的同种单质的分子,另一个分子为2个不同种原子构成的化合物分子;根据构成相同的分子为同种分子,判断该反应中共涉及四种分子;
(2)根据不同球代表不同种原子情况可判断化学反应前后判断分子的结构,可知该反应的方程式为:CH4+H2O$\frac{\underline{\;高温\;}}{\;}$CO+3H2;根据该反应中不同元素的化合价情况可知碳的化合价从+4变成+2,氢的化合价从+1、-1变到了0价,而氧的化合价没有变化,所以在该反应前后化合价发生变化有碳、氢元素;
(3)由上述分析可知该化学反应的方程式为:CH4+H2O$\frac{\underline{\;高温\;}}{\;}$CO+3H2.
故答案:(1)4;(2)碳、氢;(3)CH4+H2O $\frac{\underline{\;高温\;}}{\;}$CO+3H2.
点评 解答本题的关键是要充分理解图中的信息,掌握微观图示的结构及特点,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
6.下列不属于中和反应应用的例子是( )
| A. | 用孰石灰改良酸性土壤 | B. | 用胃舒平[含Al(OH)3]医治胃酸过多 | ||
| C. | 用盐酸除铁锈 | D. | 用烧碱溶液调节酸性过强的溶液 |
7.下列反应中,属于分解反应的是( )
| A. | H2CO3═CO2↑+H2O | B. | CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | ||
| C. | H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O | D. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 |
6.试用一种试剂将Ba(NO3)2、AgNO3、K2CO3三种溶液分开,该试剂可选用( )
| A. | 盐酸 | B. | 硝酸 | C. | 氢氧化钠 | D. | 硝酸钠 |
10.下列变化不属于化学变化的是( )
| A. | 燃放照明弹 | B. | 食物的腐烂 | C. | 工业制氧气 | D. | 钢铁的锈蚀 |
11.下列各物质属于纯净物的是( )
| A. | 空气 | B. | 海水 | C. | 氧化铜 | D. | 过氧化氢溶液 |
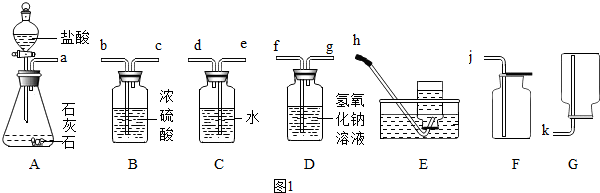

 中和反应时,很多同学对其产生探究兴趣.
中和反应时,很多同学对其产生探究兴趣.