题目内容
2.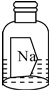 某化学兴趣小组的同学在实验台上发现一瓶标签受损的溶液,如图所示:
某化学兴趣小组的同学在实验台上发现一瓶标签受损的溶液,如图所示:【提出问题】这瓶溶液的成分是什么?
老师说:
①这瓶溶液可能是NaCl溶液、NaNO3溶液、KCl溶液、Na2CO3溶液中的一种;
②这瓶溶液中只含一种溶质.
【讨论】同学们一致认为不可能是KCl溶液.
【实验探究】实验台上可供使用的药品只有:稀HCl、稀HNO3、AgNO3溶液.请你根据以上药品完成下列实验.
| 操作步骤 | 实验现象 | 结论及化学 方程式 |
| 步骤一: 取样于试管中,然后往试管中滴加稀硝酸 | 无气泡产生 | 该溶液不是Na2CO3溶液 |
| 步骤二: 向步骤一的试管中,继续滴加AgNO3溶液 | 产生白色沉淀 | 该溶液一定是NaCl溶液,发生反应的化学方程式为 NaCl+AgNO3=AgCl↓+NaNO3 |
分析 【讨论】根据标签中物质的元素组成分析;
【实验探究】根据碳酸根离子和氯离子的鉴别方法设计方案.
【反思】根据倾倒液体时标签要向着手心,否则倾倒液体时的残留液会腐蚀标签解答.
解答 解:
【讨论】由标签知该液体含钠元素,而KCl不含钠元素,因此不可能是KCl;
【实验探究】硫酸钠和氯化钠的不同点是阴离子的不同,碳酸钠能与稀硝酸反应产生气体,而氯化钠不与稀硝酸反应,故可以使用稀硝酸与样品混合,观察有无气体产生来确定物质的成分;氯离子和银离子结合产生氯化银沉淀,因此可分别选择稀硝酸或硝酸银溶液进行鉴别;
步骤一:取样于试管中,然后往试管中滴加稀硝酸,无气泡产生,该溶液不是Na2CO3溶液;该溶液一定是NaCl溶液,发生反应的化学方程式为:NaCl+AgNO3=AgCl↓+NaNO3.
【反思】倾倒液体时标签要向着手心,否则倾倒液体时的残留液会腐蚀标签.
故答案为:
【讨论】KCl;
(2)
| 操作步骤 | 实验现象 | 结论及化学 方程式 |
| 步骤一: 取样于试管中,然后往试管中滴加稀硝酸 | 无气泡产生 | 该溶液不是 Na2CO3溶液 |
| 步骤二: 向步骤一的试管中,继续滴加 AgNO3溶液 | 产生白色沉淀 | 该溶液一定是NaCl溶液,发生反应的化学方程式为 NaCl+AgNO3=AgCl↓+NaNO3 |
点评 本题考查了破损标签试剂的确定,完成此题,可以依据破损标签的部分以及有关物质的性质进行.要求同学们熟练掌握有关物质的性质,以便灵活应用.考查了物质的组成特点及物质的性质的检验,完成此题,可以依据标签提供的物质组成特点及碳酸根离子和氯离子检验的方法进行.

练习册系列答案
相关题目
20.如图为某化学反应的微观示意图,其中相同的球代表同种原子.下列说法正确的是( )


| A. | 反应前后原子种类改变 | B. | 反应前后分子个数不变 | ||
| C. | 反应前后元素种类不变 | D. | 分子在化学变化中不可分 |
13.化学兴趣课上,同学们对过氧化钠(Na2O2)可以做供氧剂产生了浓厚兴趣,于是在老师的指导下展开了以下 探究活动.
【提供资料】①二氧化碳与过氧化钠反应生成氧气和另一种物质.
②Na2O2是一种淡黄色固体,常温下能与H2O、HCl气体等物质发生反应生成氧气,不能与N2发生反应.
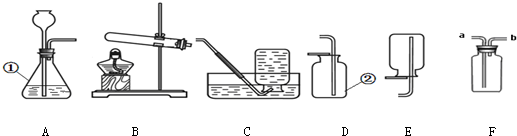
(1)探究二氧化碳与过氧化钠反应生成氧气.同学们在老师的指导下设计了如图所示装置.

①写出检验G中气体的方法将带火星木条伸入集气瓶中,若木条复燃,证明气体为氧气.
②若无装置C,对实验有影响的物质是H2O(写化学式).
③若观察到装置F不变浑浊,说明二氧化碳已经除尽.
(2)探究二氧化碳与过氧化钠反应生成的另一种物质.
【猜想与假设】下面是同学们提出的3种猜想:
猜想1:是NaOH 猜想2:是NaHCO3 猜想3:是Na2CO3
你认为猜想1、2是不正确的,理由是参加反应的物质中不含氢元素,不可能生成氢氧化钠或碳酸氢钠.
【进行实验 排除错误猜想后,同学们通过以下实验验证了另一种物质.
【反思与评价】
(3)实验之后,该小组对实验进行反思.
①某同学认为上述方案存在不足,他的理由是氧化碳与过氧化钠反应后的固体中可能含有未反应完的过氧化钠,与盐酸反应也会有气泡产生,不能证明固体中有碳酸钠.
②写出过氧化钠与二氧化碳反应的化学方程式2CO2+2Na2O2=O2+2Na2CO3.
【提供资料】①二氧化碳与过氧化钠反应生成氧气和另一种物质.
②Na2O2是一种淡黄色固体,常温下能与H2O、HCl气体等物质发生反应生成氧气,不能与N2发生反应.
(1)探究二氧化碳与过氧化钠反应生成氧气.同学们在老师的指导下设计了如图所示装置.

①写出检验G中气体的方法将带火星木条伸入集气瓶中,若木条复燃,证明气体为氧气.
②若无装置C,对实验有影响的物质是H2O(写化学式).
③若观察到装置F不变浑浊,说明二氧化碳已经除尽.
(2)探究二氧化碳与过氧化钠反应生成的另一种物质.
【猜想与假设】下面是同学们提出的3种猜想:
猜想1:是NaOH 猜想2:是NaHCO3 猜想3:是Na2CO3
你认为猜想1、2是不正确的,理由是参加反应的物质中不含氢元素,不可能生成氢氧化钠或碳酸氢钠.
【进行实验 排除错误猜想后,同学们通过以下实验验证了另一种物质.
| 实验操作 | 实验现象 |
| 取少量CO2与Na2O2反应后的固体于试管中,加入稀盐酸. | 有大量气泡产生 |
(3)实验之后,该小组对实验进行反思.
①某同学认为上述方案存在不足,他的理由是氧化碳与过氧化钠反应后的固体中可能含有未反应完的过氧化钠,与盐酸反应也会有气泡产生,不能证明固体中有碳酸钠.
②写出过氧化钠与二氧化碳反应的化学方程式2CO2+2Na2O2=O2+2Na2CO3.
10.下列工艺中主要变化属于物理变化的是( )
| A. | 造纸 | B. | 高炉炼铁 | C. | 分离液态制氧气 | D. | 煅烧石灰石 |
17.用三块相同的铝片(均已去除氧化膜)进行如下实验.
实验①:取第一块铝片,放入稀硫酸中,有明显的现象;
实验②:取第二块铝片,放入CuSO4溶液中,铝片表面有红色物质析出;
实验③:取第三块铝片,放入浓硫酸中,竟然没有明显的现象;
实验④:将实验③中的铝片取出,洗净后放入CuSO4溶液中,也没有明显现象.
下列说法不正确的是( )
实验①:取第一块铝片,放入稀硫酸中,有明显的现象;
实验②:取第二块铝片,放入CuSO4溶液中,铝片表面有红色物质析出;
实验③:取第三块铝片,放入浓硫酸中,竟然没有明显的现象;
实验④:将实验③中的铝片取出,洗净后放入CuSO4溶液中,也没有明显现象.
下列说法不正确的是( )
| A. | 铝片与浓硫酸不能发生化学反应 | B. | 实验①观察到铝片表面有气泡产生 | ||
| C. | 由实验②可以得出金属铝比铜活泼 | D. | 浓硫酸与稀硫酸的化学性质有差别 |
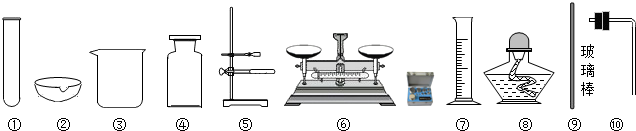
 Ⅰ.今年湄公河流域遭遇百年干旱,中国克服困难伸援手开闸放水,使湄公河沿岸的早情得到极大缓解.请回答下列问题:
Ⅰ.今年湄公河流域遭遇百年干旱,中国克服困难伸援手开闸放水,使湄公河沿岸的早情得到极大缓解.请回答下列问题: