题目内容
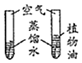
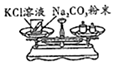
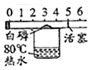
3.下列实验方案能达到目的是( )| A、探究二氧化锰对反应速率的影响 | B、探究铁生锈与水有关 | C、探究质量守恒定律 | D、测定空气中氧气的含量 |
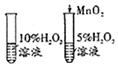 |  |  |  |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
分析 A、要注意变量的控制,注意要除探究要素不同之外,其它条件都应该是相同的,据此进行分析判断.
B、根据铁锈蚀的条件,进行分析判断.
C、验证质量守恒定律的实验时,选用药品和装置应考虑:①只有质量没有变化的化学变化才能直接用于验证质量守恒;②如果反应物中有气体参加反应,或生成物中有气体生成,应该选用密闭装置.
D、根据测定空气中氧气含量的实验原理,进行分析判断.
解答 解:A、由于过氧化氢溶液的浓度不同,无法确定二氧化锰对反应速率的影响,故选项实验方案不能达到目的.
B、第一支试管的铁能与氧气、水接触,第二支试管中的铁只能与水接触,不能探究铁生锈是否与水有关,故选项实验方案不能达到目的.
C、氯化钾溶液与碳酸钠粉末不反应,不能用于探究质量守恒定律,故选项实验方案不能达到目的.
D、白磷燃烧消耗氧气,使注射器内的气体减少,减少的气体就是氧气的体积,故选项实验方案能达到目的.
故选:D.
点评 本题难度不是很大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体解题时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列图示基本实验操作中,正确的是( )
| A. | 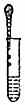 滴加液体 | B. | 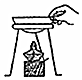 移走蒸发皿 | C. |  收集氧气 | D. |  闻药品气味 |
8.生活中的下列变化,属于化学变化的是( )
| A. | 冰雪融化 | B. | 钢铁生锈 | C. | 汽油挥发 | D. | 铁铸成锅 |
15.下列物质能和氢氧化钡溶液、稀盐酸、氯化钙溶液都反应的是( )
| A. | 氯化钠溶液 | B. | 硫酸铜溶液 | C. | 碳酸钠溶液 | D. | 碳酸钙 |
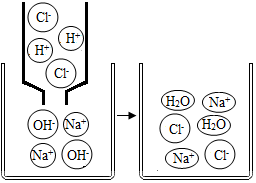 如图是氢氧化钠与盐酸发生反应的微观示意图.
如图是氢氧化钠与盐酸发生反应的微观示意图.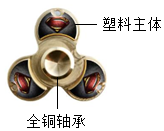 指尖陀螺是一种可以在手指上空转的小玩具.它的结构如图所示:
指尖陀螺是一种可以在手指上空转的小玩具.它的结构如图所示: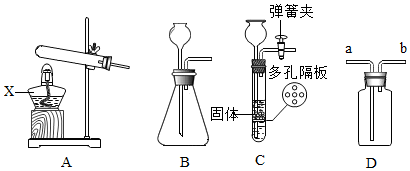 如图是实验室制取气体的部分装置.
如图是实验室制取气体的部分装置.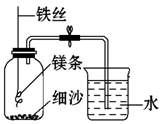 化学学习小组用金属镁进行实验探究.
化学学习小组用金属镁进行实验探究.