题目内容
化学兴趣小组对“锌与稀硫酸反应快慢的影响因素”进行了探究.
【提出问题】锌与稀硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a、可能与稀硫酸的溶质质量分数有关;
b、可能与锌的形状有关.
【设计并实验】兴趣小组用100mL不同质量分数的稀硫酸和5g不同形状的锌进行如下实验(时间为3分钟).
(1)用图1所示装置收集并测量氢气的体积,其中量筒的作用是 ,氢气应从 (填e或f或g)管通入.
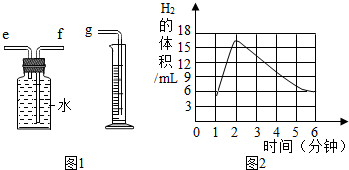
【收集证据】
(2)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是 .
【得出结论】
(3)结论是 .
【拓展延伸】
(4)如图是兴趣小组第①组实验根据前6分钟记录详细数据所绘制的曲线(每分钟记录一次产生氢气的体积),请解释锌与稀硫酸反应由快变慢的原因 .
(5)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证.
因素影响: 、
简述实验验证的方法: .
【提出问题】锌与稀硫酸反应的快慢受哪些因素的影响呢?
【猜想与假设】a、可能与稀硫酸的溶质质量分数有关;
b、可能与锌的形状有关.
【设计并实验】兴趣小组用100mL不同质量分数的稀硫酸和5g不同形状的锌进行如下实验(时间为3分钟).
| 实验编号 | 硫酸的质量分数(均取200mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3分钟) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |

【收集证据】
(2)要比较不同质量分数的硫酸对反应快慢的影响,应选择的实验编号是
【得出结论】
(3)结论是
【拓展延伸】
(4)如图是兴趣小组第①组实验根据前6分钟记录详细数据所绘制的曲线(每分钟记录一次产生氢气的体积),请解释锌与稀硫酸反应由快变慢的原因
(5)锌与硫酸反应的快慢可能还受哪些因素影响?设计实验验证.
因素影响:
简述实验验证的方法:
考点:影响化学反应速率的因素探究,金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)为测定所收集氢气的体积,则需要采用液体等量代换的方式,因此可以选用右图这样的装置,短进长出,让里面的水等量流到量筒内,通过量筒内液体的体积判断收集的气体的体积;
(2)对比四个实验,利用控制变量法选择合适的对比组;
(3)通过不同质量分数的硫酸或不同形状的锌的产生氢气的快慢得出结论;
(4)根据表格的数据总结产生的氢气与时间的关系并分析原因;
(5)反应物浓度、反应温度、反应物接触面积、有无催化剂等因素常影响化学反应速率,利用控制变量的思想设计一个因素对反应速率的影响.
(2)对比四个实验,利用控制变量法选择合适的对比组;
(3)通过不同质量分数的硫酸或不同形状的锌的产生氢气的快慢得出结论;
(4)根据表格的数据总结产生的氢气与时间的关系并分析原因;
(5)反应物浓度、反应温度、反应物接触面积、有无催化剂等因素常影响化学反应速率,利用控制变量的思想设计一个因素对反应速率的影响.
解答:解:(1)因为氢气不易溶于水,可以通过压强的变化利用排水法把水压入量筒内,根据进入量筒中水的体积,判断生成氢气的体积,故进气管是短管e;故填:根据进入量筒中水的体积,判断生成氢气的体积;e;
(2)要比较不同质量分数的硫酸对反应快慢的影响,其中的锌的状态保持不变,选择不同质量分数的硫酸,看产生氢气的快慢,因此可以选择①③(都是锌粒)或②④(都是锌片);故填:①③或②④;
(3)通过①③(都是锌粒,硫酸的质量分数不同),可以看出:硫酸的质量分数越大,反应速率越快;通过①②(锌粒和锌片与质量分数相同的硫酸反应)可以看出:锌与硫酸的接触面积越大,反应速率越快;故填:硫酸的质量分数越大,反应速率越快或锌与硫酸的接触面积越大,反应速率越快;
(4)从表格可以看出反应由慢到快然后逐渐减慢;因为随着反应的进行,反应放出热量,反应速度加快,但随着硫酸被消耗,硫酸溶质质量分数变小,反应速度又逐渐减慢;
故填:随着硫酸被消耗,硫酸溶质质量分数变小,反应速度又逐渐减慢;
(5)如设计温度对反应快慢的影响,具体的操作为:取质量相等的锌粒分别放入两只试管中,然后分别加入温度不同,体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间.(只要有控制变量的意识即可);
故填:温度;取质量相等的锌粒分别放入两只试管中,然后分别加入温度不同,体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间.(只要有控制变量的意识即可).
(2)要比较不同质量分数的硫酸对反应快慢的影响,其中的锌的状态保持不变,选择不同质量分数的硫酸,看产生氢气的快慢,因此可以选择①③(都是锌粒)或②④(都是锌片);故填:①③或②④;
(3)通过①③(都是锌粒,硫酸的质量分数不同),可以看出:硫酸的质量分数越大,反应速率越快;通过①②(锌粒和锌片与质量分数相同的硫酸反应)可以看出:锌与硫酸的接触面积越大,反应速率越快;故填:硫酸的质量分数越大,反应速率越快或锌与硫酸的接触面积越大,反应速率越快;
(4)从表格可以看出反应由慢到快然后逐渐减慢;因为随着反应的进行,反应放出热量,反应速度加快,但随着硫酸被消耗,硫酸溶质质量分数变小,反应速度又逐渐减慢;
故填:随着硫酸被消耗,硫酸溶质质量分数变小,反应速度又逐渐减慢;
(5)如设计温度对反应快慢的影响,具体的操作为:取质量相等的锌粒分别放入两只试管中,然后分别加入温度不同,体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间.(只要有控制变量的意识即可);
故填:温度;取质量相等的锌粒分别放入两只试管中,然后分别加入温度不同,体积和溶质质量分数相同的稀硫酸,测量收集等体积的氢气所需要的时间.(只要有控制变量的意识即可).
点评:本题以影响产生氢气的反应速率为实验探究的形式考查了反应物浓度、颗粒的大小、反应温度等因素对化学反应速率的影响,重点在于培养学生的实验探究能力,注意控制变量的运用.

练习册系列答案
相关题目
下列物质的用途,主要利用其化学性质的是( )
A、 |
B、 |
C、 |
D、 |
下列鉴别物质的方法,不正确的是( )
| A、用灼烧的方法区分羊毛和棉线 |
| B、区分空气和氧气的最佳方法是测气体密度 |
| C、用熟石灰区分铵态氮肥和尿素 |
| D、采用相互刻划的方法比较合金和纯金属的硬度 |

 溶液不是NaNO3,为确定其成分,某同学进行如下研究.
溶液不是NaNO3,为确定其成分,某同学进行如下研究.
 丹丹和东东两位同学在阅读教材中的【查阅资料】草木灰的主要成分是碳酸钾,碳酸钾的化学性质和碳酸钠的化学性质相似.
丹丹和东东两位同学在阅读教材中的【查阅资料】草木灰的主要成分是碳酸钾,碳酸钾的化学性质和碳酸钠的化学性质相似.