题目内容
16.在做中和反应实验时,我将稀盐酸滴入氢氧化钠溶液中,意外地看到有气泡产生.我认为是氢氧化钠溶液变质了.(1)氢氧化钠溶液变质的原因是CO2+2NaOH=Na2CO3+H2O(化学方程式).
(2)利用与上述实验不同的原理,我又设计了一个实验再次确认该氢氧化钠溶液已变质:
| 实 验 步 骤 | 实 验 现 象 | 实 验 结 论 |
| 取少量氢氧化钠溶液于 试管中,滴加氯化钙溶液 | 溶液中产生白色沉淀 | 该氢氧化钠溶液 已变质 |
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量溶液于试管中,滴加足量的氯化钡溶液. | 白色沉淀 | 该氢氧化钠溶液已 部分变质 |
| (2)上述溶液过滤,取滤液滴加无色酚酞 试液. | 溶液变红 |
分析 (1)氢氧化钠能与二氧化碳发生反应生成水和碳酸钠,瓶口残留的氢氧化钠溶液吸收空气中的二氧化碳而变质;
(2)在前面使用了稀盐酸与碳酸钠反应放出气体二氧化碳检验氢氧化钠的变质;碳酸钠还可以与氯化钙等形成白色沉淀,而氢氧化钠不能与氯化钙反应,因此,可根据这个性质检验氢氧化钠的变质;
(3)如果氢氧化钠全部变质则溶液为碳酸钠溶液,若部分变质则溶液为氢氧化钠与碳酸钠的混合溶液;因此,需要选用氯化钡等溶液除去溶液中的碳酸钠后,使用无色酚酞检验是否存在氢氧化钠,以确定是全部变质还是部分变质.
解答 解:(1)氢氧化钠溶液吸收空气中的二氧化碳生成碳酸钠和水,因此,与空气接触的氢氧化钠溶液会变质,化学方程式为:CO2+2NaOH=Na2CO3+H2O;
(2)碳酸盐和酸反应有气体生成,和含Ba2+(或Ca2+)的溶液反应会生成沉淀;
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量NaOH溶液与试管中,滴加氯化钙溶液 | 溶液中产生白色沉淀 | 该氢氧化钠已变质 |
| 实验步骤 | 实验现象 | 实验结论 |
| (1)取少量溶液于试管中,滴加足量的氯化钡溶液. | 白色沉淀 | 该氢氧化钠溶液已 部分变质 |
| (2)上述溶液过滤,取滤液滴加无色酚酞 试液. | 溶液变红 |
(2)
| 实验步骤 | 实验现象 | 实验结论 |
| 溶液中产生白色沉淀 |
| 实验步骤 | 实验现象 | 实验结论 |
| 氯化钡 | 白色沉淀 | |
| 无色酚酞 |
点评 本题在探究时具有较好的开放性,选择的试剂不唯一,学生可能有不同的答案,只要设计合理,现象明显,结论正确都是正确答案.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
11.下列常用物质中,属于纯净物的是( )
| A. | 牛奶 | B. | 过氧化氢溶液 | C. | 纯净水 | D. | 冰水混合物 |
4.小明对所学知识进行归纳,其中有错误的一组是( )
| A. | 常见干燥剂:烧碱、浓硫酸、石灰石 | |
| B. | 常见的合金:不锈钢、黄铜、生铁 | |
| C. | 常见营养物质:蛋白质、无机盐、维生素 | |
| D. | 常见的材料:金属材料、无机非金属材料、有机合成材料 |
11.不同的条件和环境,对材料的物理性质要求不同.消防队员所穿的消防服就应具备某些特殊性质,若让你设计消防服,对选用的材料应具备的性质提出要求中错误的是( )
| A. | 耐腐蚀,防化学品 | B. | 不导电,防电源漏电触电 | ||
| C. | 不善于传热、阻燃、熔点高 | D. | 红色,便于发现消防队员的位置 |
1. 哈尔滨地铁1号线所用B型车通常采用铝合金和不锈钢.下列有关铝合金和不锈钢的说法中不正确的是( )
哈尔滨地铁1号线所用B型车通常采用铝合金和不锈钢.下列有关铝合金和不锈钢的说法中不正确的是( )
 哈尔滨地铁1号线所用B型车通常采用铝合金和不锈钢.下列有关铝合金和不锈钢的说法中不正确的是( )
哈尔滨地铁1号线所用B型车通常采用铝合金和不锈钢.下列有关铝合金和不锈钢的说法中不正确的是( )| A. | 不锈钢除含铁外还含有少量的铬、镍等 | |
| B. | 铝合金和不锈钢都具有很好的抗腐蚀性能 | |
| C. | 铝合金和不锈钢都是合金,合金中可能含有非金属 | |
| D. | 合金的硬度比组成它的纯金属大,熔点比纯金属高 |
8.乙醇是重要的化工原料.下列有关叙述正确的是( )
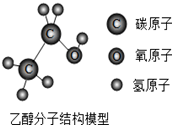

| A. | 乙醇分子是由碳、氢、氧元素组成 | |
| B. | 乙醇是由碳原子、氢原子、氧原子构成 | |
| C. | 乙醇中质子数和电子数的比是1:1 | |
| D. | 每个乙醇分子中都含有8个原子核 |