题目内容
7.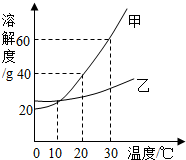 如图是甲、乙两种固体物质的溶解度曲线,请根据图回答下列问题.
如图是甲、乙两种固体物质的溶解度曲线,请根据图回答下列问题.(1)30℃时,将80g甲物质加入100g水中,充分溶解后能得到溶液的质量为160g.
(2)10℃时,甲、乙两种物质的溶液中溶解度相等.
(3)当甲物质中含有少量的乙物质时,用冷却热饱和溶液方法(填“蒸发溶剂”或”冷却热饱和溶液”)来提纯甲物质.
分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;30℃时,甲的溶解度是60g,因此将80g甲物质加入100g水中,充分溶解后能得到溶液的质量为160g;10℃时,甲、乙两种物质的溶液中溶解度相等,因为在该温度下,两种物质有交点;当甲物质中含有少量的乙物质时,用冷却热饱和溶液的方法来提纯甲物质,因为甲的溶解度随温度的升高变化比乙大.
解答 解:(1)30℃时,甲的溶解度是60g,因此将80g甲物质加入100g水中,充分溶解后能得到溶液的质量为160g;故答案为:160g;
(2)10℃时,甲、乙两种物质的溶液中溶解度相等,因为在该温度下,两种物质有交点,故答案为:10;
(3)当甲物质中含有少量的乙物质时,用冷却热饱和溶液的方法来提纯甲物质,因为甲的溶解度随温度的升高变化比乙大;故答案为:冷却热饱和溶液
点评 本考点考查了溶解度曲线及其应用、配制溶液和实验数据的处理问题,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
相关题目
18.如图是对四个实验绘制的图形,其中实验结果与图形对应准确的是( )
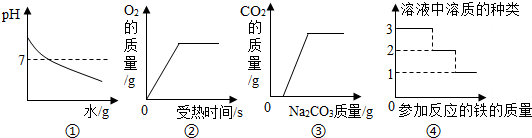

| A. | 图①是pH=13的NaOH溶液中加水稀释 | |
| B. | 图②是用适量的KClO3和MnO2混合物加热制O2 | |
| C. | 图③是向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| D. | 图④向Cu(NO3)2和AgNO3的混合溶液中加入铁粉至过量 |
15.下列变化属于化学变化的是( )
| A. | 百炼成钢 | B. | 积水成渊 | C. | 铁杵成针 | D. | 滴水成冰 |
2.观察是学习化学的一种方法.下列有关实验现象描述正确的是( )
| A. | 铜丝在空气中灼烧一段时间,铜丝加热变蓝 | |
| B. | 铁丝在氧气中剧烈燃烧、火星四射、生成白色固体 | |
| C. | 分别点燃一小块棉纤维和羊毛纤维,都产生了烧焦羽毛的气味 | |
| D. | 将一块生石灰投入到装有适量水的烧杯中,一段时间后烧杯外壁发烫 |
19.根据如图有关信息判断,下列说法错误的是( )
| A. |  镁离子(Mg2+)核内有12个质子 | |
| B. |  镁的相对原子质量为24.31 | |
| C. |  镁离子与硫离子的最外层电子数相等 | |
| D. |  在化学反应中,硫原子容易失去2个电子 |
17.某同学在实验结束后进行废液处理时,将氢氧化钠溶液、石灰水和稀盐酸导入同一洁净的烧杯中,当他用手接触烧杯壁时,感觉到烧杯“发热”.这一现象让他意识到酸碱发生了中和反应.为了找到处理这类废液的依据,他决定探究反应后溶液中溶质的组成.
【猜想假设】他对反应后溶液中溶质的组成作出了两种假设.
假设①:溶质为NaCl、CaCl2
假设②:溶质为NaCl、CaCl2、NaOH、Ca(OH)2
请你再补充一种合理的假设.
假设③:溶质为NaCl、CaCl2、HCl.
【设计方案】如果假设③成立,请你根据下表实验方案,验证探究结果.
请写出其中任一套方案所发生的化学反应方程式:Fe+2HCl=FeCl2+H2↑或Na2CO3+2HCl=2NaCl+H2O+CO2↑;
【拓展应用】
(1)处理含酸碱的废液时,调控废液至上述假设①的状态最合适;
(2)假如运送硫酸的车辆在公路旁发生泄漏事故,为减轻硫酸对周边环境的危害,可采取的措施是喷洒石灰水.
【猜想假设】他对反应后溶液中溶质的组成作出了两种假设.
假设①:溶质为NaCl、CaCl2
假设②:溶质为NaCl、CaCl2、NaOH、Ca(OH)2
请你再补充一种合理的假设.
假设③:溶质为NaCl、CaCl2、HCl.
【设计方案】如果假设③成立,请你根据下表实验方案,验证探究结果.
| 实验步骤及操作方法 | 实验现象 | 结论 |
| 方案一:取少量废液于试管中,加入适量铁粉,振荡 | 铁粉消失,并有气泡产生 | 假设③成立 |
| 方案二:取少量废液于试管中,滴加一定量 碳酸钠溶液,振荡 | 有大量气泡产生 | 假设③成立 |
【拓展应用】
(1)处理含酸碱的废液时,调控废液至上述假设①的状态最合适;
(2)假如运送硫酸的车辆在公路旁发生泄漏事故,为减轻硫酸对周边环境的危害,可采取的措施是喷洒石灰水.