题目内容
反应8NH3+3Cl2=6NH4Cl+N2中,若有10.2g NH3被氧化,则反应用去的氯气在标准状况下体积是
- A.5.04L
- B.20.16L
- C.6.72L
- D.13.44L
B
分析:化合价升高是被氧化,所以通过方程式可知8个氨分子中只有2个氨分子被氧化,同时消耗氯气3个分子,再根据10.2g NH3算出氨分子的物质的量,通过氨分子的物质量算出氯气的物质的量,再根据摩尔体积算出氯气的体积.
解答:10.2g NH3的物质的量为: =0.6摩尔,由于2分子氨分子被氧化需要消耗3个氯分子,所以0.6摩尔氨分子被氧化,需要氯分子0.9摩尔,所以氯气的体积为0.9摩尔×22.4升/摩=20.16升.
=0.6摩尔,由于2分子氨分子被氧化需要消耗3个氯分子,所以0.6摩尔氨分子被氧化,需要氯分子0.9摩尔,所以氯气的体积为0.9摩尔×22.4升/摩=20.16升.
故选B.
点评:要熟悉质量与物质的量的换算关系:物质的量=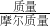 ,物质的量与体积关系:物质的量=
,物质的量与体积关系:物质的量= .
.
分析:化合价升高是被氧化,所以通过方程式可知8个氨分子中只有2个氨分子被氧化,同时消耗氯气3个分子,再根据10.2g NH3算出氨分子的物质的量,通过氨分子的物质量算出氯气的物质的量,再根据摩尔体积算出氯气的体积.
解答:10.2g NH3的物质的量为:
 =0.6摩尔,由于2分子氨分子被氧化需要消耗3个氯分子,所以0.6摩尔氨分子被氧化,需要氯分子0.9摩尔,所以氯气的体积为0.9摩尔×22.4升/摩=20.16升.
=0.6摩尔,由于2分子氨分子被氧化需要消耗3个氯分子,所以0.6摩尔氨分子被氧化,需要氯分子0.9摩尔,所以氯气的体积为0.9摩尔×22.4升/摩=20.16升.故选B.
点评:要熟悉质量与物质的量的换算关系:物质的量=
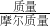 ,物质的量与体积关系:物质的量=
,物质的量与体积关系:物质的量= .
. 
练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
反应8NH3+3Cl2=6NH4Cl+N2中,若有10.2g NH3被氧化,则反应用去的氯气在标准状况下体积是( )
| A、5.04L | B、20.16L | C、6.72L | D、13.44L |