题目内容
13. 实验室里可用二氧化锰催化分解过氧化氢溶液或加热氯酸钾或加热高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
实验室里可用二氧化锰催化分解过氧化氢溶液或加热氯酸钾或加热高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.【探究之一】
某同学用如图所示装置制取氧气,则其反应原理是(用化学方程式表示)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
【探究之二】
还有没有其它物质可以催化分解过氧化氢?
【查阅资料】
CuSO4溶液、动物某些脏器中的过氧化氢酶等物质能催化过氧化氢的分解.
【问题思考】
(1)动物脏器中的过氧化氢酶是蛋白质(选填糖类、蛋白质、脂肪或维生素).
(2)CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42-),那CuSO4溶液中究竟是哪种粒子能起催化作用呢?
(3)大家一致认为不可能是H2O,理由是过氧化氢溶液的溶剂是水,若水是催化剂,过氧化氢早已分解完毕了,所以H2O不是催化剂.
【实验验证】
为进一步验证另外的两种粒子是否起到催化作用,小红同学设计了如表实验,完成了这次探究活动.
| 实验步骤 | 实验现象 | 结论 |
| a、取一支试管加入5ml 5%过氧化氢溶液,然后加入2~3滴稀硫酸溶液 | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是铜离子. |
| b、另取一支试管加入5ml5%过氧化氢溶液,然后加入2~3滴CuSO4(或硫酸铜)溶液. | 溶液中有大量气泡放出 |
如果要确定CuSO4是催化剂,还必须通过实验确定它在化学反应前后化学性质和质量都没有发生改变.
分析 如果用过氧化氢和二氧化锰制氧气,就不需要加热;如果用高锰酸钾或氯酸钾就需要加热.氧气不易溶于水,密度比空气的密度大,因此可以用排水法和向上排空气法收集,排水法收集的气体比较纯净.酶属于蛋白质;小红同学认为最不可能的是H2O,他的理由是:过氧化氢溶液中的溶剂是水,因此H2O不能起催化作用;滴稀硫酸无变化,证明了硫酸根离子不能做催化剂;滴硫酸铜时,有大量气泡放出,证明了起催化作用的是铜离子;催化剂是指能改变其他物质的化学反应速率,而本身的质量和化学性质在化学反应前后都不变的物质.
解答 解:【探究之一】过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,发生的化学反应方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
【问题思考】(1)过氧化氢酶属于蛋白质;故填:蛋白质;
(3)认为最不可能的是H2O,他的理由是:过氧化氢溶液中的溶剂是水,因此H2O不能起催化作用;故填:过氧化氢溶液的溶剂是水,若水是催化剂,过氧化氢早已分解完毕了,所以H2O不是催化剂;
【实验验证】
滴稀硫酸无变化,证明了硫酸根离子不能做催化剂;滴硫酸铜时,有大量气泡放出,证明了起催化作用的是铜离子;故填:CuSO4(或硫酸铜);铜离子;
【实验反思】催化剂是指能改变其他物质的化学反应速率,而本身的质量和化学性质在化学反应前后都不变的物质.故填:化学性质和质量都没有发生改变.
点评 本考点主要考查氧气的制取装置,同时也考查了催化剂的特点和化学方程式的书写,综合性比较强.本考点是中考的重要考点之一,主要出现在实验探究题中.

练习册系列答案
相关题目
4.下列说法正确的是( )
| A. | 物质和氧气发生的反应是氧化反应,所以发生氧化反应一定有氧气参加 | |
| B. | 合金的硬度大于各成分金属,所以黄铜的硬度大于紫铜 | |
| C. | 可燃物燃烧时温度需要达到着火点,所以可燃物的温度达到着火点一定能燃烧 | |
| D. | 单质一定是由一种元素组成的,所以由一种元素组成的物质一定是单质 |
8.高锰酸钾受热分解可得到锰酸钾(K2MnO4),则锰酸钾中锰元素的化合价为( )
| A. | +2 | B. | +4 | C. | +6 | D. | +7 |
5.如表是NaCl、KNO3在不同温度时的溶解度,据此数据,判断下列说法错误的是( )
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
| A. | KNO3和NaCl的溶解度曲线在20℃-30℃温度范围内会相交 | |
| B. | 在60℃时,KNO3的饱和溶液105g加入95g水后,溶液中溶质的质量分数为27.5% | |
| C. | 在20℃时,NaCl和KNO3固体各35g分别加入两只各盛有100g水的烧杯中,均不能形成饱和溶液 | |
| D. | 从含有少量NaCl的KNO3饱和溶液中得到较多的KNO3晶体,通常可采用冷却热饱和溶液的方法 |
2.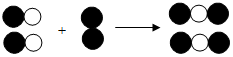 如图,该图能体现的知识有( )
如图,该图能体现的知识有( )
①质量守恒定律;
②化合物分子是由不同原子构成的;
③在化学反应中分子的种类发生了改变;
④该反应可能是氢气与氧气的反应.
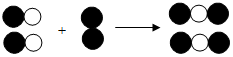 如图,该图能体现的知识有( )
如图,该图能体现的知识有( )①质量守恒定律;
②化合物分子是由不同原子构成的;
③在化学反应中分子的种类发生了改变;
④该反应可能是氢气与氧气的反应.
| A. | ①②③④ | B. | ①②③ | C. | ②③④ | D. | ②③ |