题目内容
5.为控制日益严重的温室效应,科学家采取“组合转化”技术,将CO2和H2混合生成一种重要的化工产品R和水:2CO2+6H2═R+4H2O,则R化学式为( )| A. | CH | B. | C2H2 | C. | CH2 | D. | C2H4 |
分析 由题意,已知反应物和生产物,根据质量守恒定律:原子的个数反应前后不变,查各种原子的个数.
解答 解:已知反应物和生产物,根据质量守恒定律:原子的个数反应前后不变;查各种原子反应前后的个数.R化学式为C2H4.
点评 反应前后原子的种类和数目不变.

练习册系列答案
相关题目
15.下列物质暴露于空气中,其质量改变和空气中的成分没有关系的是( )
| A. | 生石灰 | B. | 铁粉 | C. | 浓硫酸 | D. | 浓盐酸 |
16.下列说法正确的是( )
①向某无色溶液中滴加紫色石蕊试液变蓝色,说明该溶液是碱性溶液
②铜丝浸入硝酸汞溶液中,表面覆盖一层银白色的物质,说明铜比汞活泼
③在某固体中滴加稀盐酸,有气泡产生,说明该固体是碳酸盐
④向某无色溶液中滴加氯化钡溶液,产生白色沉淀,说明该溶液是硫酸溶液.
①向某无色溶液中滴加紫色石蕊试液变蓝色,说明该溶液是碱性溶液
②铜丝浸入硝酸汞溶液中,表面覆盖一层银白色的物质,说明铜比汞活泼
③在某固体中滴加稀盐酸,有气泡产生,说明该固体是碳酸盐
④向某无色溶液中滴加氯化钡溶液,产生白色沉淀,说明该溶液是硫酸溶液.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
10.某化学小组用熟石灰配制石灰水时,发现装满熟石灰的塑料试剂瓶已经破埙.
【提出向题1】试剂是否变质?
【猜想】
①没有变质,成分是氢氧化钙
②全部变质,成分是碳酸钙
③部分变质,成分是氢氧化钙和碳酸钙
【进行实验1】
【提出问题2】如何测定试剂中碳酸钙的质量分数?
【进行实验2】小丽同学设计了如图所示装置进行碳酸钙的质量分数测定:
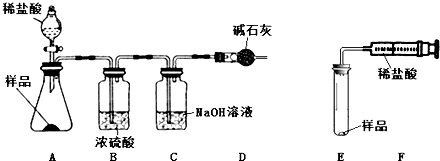
取一定质量的样品放入锥形瓶中,加入过量稀盐酸(不考虑稀盐酸的挥发),测量装置C在反应前后的总质量,即可计算出试剂中碳酸钙的质量分数.请写出稀盐酸与碳酸钙发生反应的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑
说明:装置气密性良好,操作无误,各步反应完全.
【反思与评价】
(1)小文同学认为小丽得到的结果有较大的误差,理由是装置中的二氧化碳能够被C中的氢氧化钠溶液吸收,导致测定结果偏大
(2)小文同学用图E、F所示装置(注射器活塞的摩擦力很小,忽略不计)完成测量.注射器除了贮存、加注稀盐酸外,还有的作用是测定反应生成二氧化碳的体积
【交流与讨论】
实验结束后将A、C、E中废液倒入一个干净的废液缸中,观察到有沉淀生成.
(1)同学们将废液过滤并讨论滤液中溶质的成分,该滤液中一定存在的溶质是氯化钠
(2)经实验确认废液成分,处理后绿色排放.
【提出向题1】试剂是否变质?
【猜想】
①没有变质,成分是氢氧化钙
②全部变质,成分是碳酸钙
③部分变质,成分是氢氧化钙和碳酸钙
【进行实验1】
| 步骤 | 操 作 | 现 象 | 结论 |
| 1 | 取样品于试管中,加水,滴入2~3滴酚酞试液 | 酚酞试液变红色 | 猜想③正确 |
| 2 | 向试管中继续加入过量的稀盐酸 | 产生气泡 |
【进行实验2】小丽同学设计了如图所示装置进行碳酸钙的质量分数测定:

取一定质量的样品放入锥形瓶中,加入过量稀盐酸(不考虑稀盐酸的挥发),测量装置C在反应前后的总质量,即可计算出试剂中碳酸钙的质量分数.请写出稀盐酸与碳酸钙发生反应的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑
说明:装置气密性良好,操作无误,各步反应完全.
【反思与评价】
(1)小文同学认为小丽得到的结果有较大的误差,理由是装置中的二氧化碳能够被C中的氢氧化钠溶液吸收,导致测定结果偏大
(2)小文同学用图E、F所示装置(注射器活塞的摩擦力很小,忽略不计)完成测量.注射器除了贮存、加注稀盐酸外,还有的作用是测定反应生成二氧化碳的体积
【交流与讨论】
实验结束后将A、C、E中废液倒入一个干净的废液缸中,观察到有沉淀生成.
(1)同学们将废液过滤并讨论滤液中溶质的成分,该滤液中一定存在的溶质是氯化钠
(2)经实验确认废液成分,处理后绿色排放.
15.下列物质中,属于混合物的是( )
| A. | 氯酸钾 | B. | 氧气 | C. | 氧化镁 | D. | 海水 |
 请根据常见金属的活动性顺序回答.
请根据常见金属的活动性顺序回答.