题目内容
现有银、铜、铁三种金属,某研究小组的同学为探究银、铜、铁的金属活动性顺序,
设计了三个实验:I.将铁片浸入稀硫酸中;Ⅱ.将银片浸入稀硫酸中;Ⅲ.将铁片浸入硫酸铜溶液中.
(1)实验I的现象是:有气泡产生,溶液由无色逐渐变为浅绿色.反应的化学方程式为 ;反应产生的气体可用 的方法检验.
(2)上述三个实验还不能完全证明三种金属的活动性顺序,请你补充一个实验来达到实验目的(写出实验操作和现象) .根据以上探究,三种金属的活动性由强到弱的顺序是 .
(3)将银、铜、铁中的银、铁两种金属分别放入 溶液中,即可验证这三种金属的活动性强弱.
设计了三个实验:I.将铁片浸入稀硫酸中;Ⅱ.将银片浸入稀硫酸中;Ⅲ.将铁片浸入硫酸铜溶液中.
(1)实验I的现象是:有气泡产生,溶液由无色逐渐变为浅绿色.反应的化学方程式为
(2)上述三个实验还不能完全证明三种金属的活动性顺序,请你补充一个实验来达到实验目的(写出实验操作和现象)
(3)将银、铜、铁中的银、铁两种金属分别放入
考点:金属活动性的探究,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据铁与稀硫酸反应,写出反应的方程式,根据氢气的可燃性分析检验的方法;
(2)分析上述三个实验,还不能比较铜和银活泼性,所以只要设计的实验能比较出二者的活泼性就行;
(3)根据金属与盐反应的条件考虑;
(2)分析上述三个实验,还不能比较铜和银活泼性,所以只要设计的实验能比较出二者的活泼性就行;
(3)根据金属与盐反应的条件考虑;
解答:解:(1)铁与稀硫酸反应,生成了硫酸亚铁和氢气,反应的方程式是:Fe+H2SO4=FeSO4+H2↑,氢气还具有可燃性,可用燃着的木条来检验,气体能燃烧产生了淡蓝色的火焰;
(2)将铁片浸入稀硫酸中能产生氢气,说明铁排在氢的前面;将银片浸入稀硫酸中,不反应说明银排在氢的后面;将铁片浸入硫酸铜溶液中铁的表面有红色固体析出,说明铁比铜活泼.但铜和银不能比较,所以将铜丝伸入硝酸银溶液中,铜丝的表面覆盖一层银白色的物质,溶液由无色变为蓝色.说明铜比银活泼;所以,三种金属的活动性由强到弱的顺序是铁、铜、银.
(3)金属与盐反应说明金属排在盐中金属的前面,金属与盐不反应,说明金属排在了盐中金属的后面,所以加入的盐溶液应该位于两种金属之间;由于铜在中间,所以两种金属放到硫酸铜溶液中即可;
答案:(1)Fe+H2SO4=FeSO4+H2↑,燃着的木条来检验,气体能燃烧产生了淡蓝色的火焰;(2)将铜丝伸入硝酸银溶液中,铜丝的表面覆盖一层银白色的物质,溶液由无色变为蓝色,铁、铜、银;(3)硫酸铜.
(2)将铁片浸入稀硫酸中能产生氢气,说明铁排在氢的前面;将银片浸入稀硫酸中,不反应说明银排在氢的后面;将铁片浸入硫酸铜溶液中铁的表面有红色固体析出,说明铁比铜活泼.但铜和银不能比较,所以将铜丝伸入硝酸银溶液中,铜丝的表面覆盖一层银白色的物质,溶液由无色变为蓝色.说明铜比银活泼;所以,三种金属的活动性由强到弱的顺序是铁、铜、银.
(3)金属与盐反应说明金属排在盐中金属的前面,金属与盐不反应,说明金属排在了盐中金属的后面,所以加入的盐溶液应该位于两种金属之间;由于铜在中间,所以两种金属放到硫酸铜溶液中即可;
答案:(1)Fe+H2SO4=FeSO4+H2↑,燃着的木条来检验,气体能燃烧产生了淡蓝色的火焰;(2)将铜丝伸入硝酸银溶液中,铜丝的表面覆盖一层银白色的物质,溶液由无色变为蓝色,铁、铜、银;(3)硫酸铜.
点评:解答本题关键是要知道方程式的写法,尤其是要知道铁与硫酸反应升成硫酸亚铁;根据金属与盐反应说明金属排在盐中金属的前面,金属与盐不反应,说明金属排在了盐中金属的后面,再进一步进行分析即可.

练习册系列答案
相关题目
将下列固体分别放入水中,所形成的分散系温度明显降低的是( )
| A、硝酸铵 | B、生石灰 |
| C、氢氧化钠 | D、食盐 |
下列图示的实验操作中,不正确的是( )
A、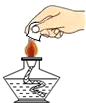 熄灭酒精灯 |
B、 称取氯化钠固体 |
C、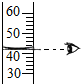 读取液体体积 |
D、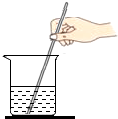 溶解氯化钠 |
下列叙述错误的是( )
| A、分子在不停的运动 |
| B、原子之间也有间隔 |
| C、原子和分子都可以直接构成物质 |
| D、化学变化中原子和分子都可以分裂 |
下列变化不包含缓慢氧化的是( )
| A、农家肥料的腐熟 |
| B、动植物的呼吸 |
| C、酒和醋的酿造 |
| D、酒精的挥发 |
 小明家养鱼购进了一批鱼池增氧剂--颗粒氧(如图)引起了小明的探究兴趣.
小明家养鱼购进了一批鱼池增氧剂--颗粒氧(如图)引起了小明的探究兴趣. 铬(Cr)元素与人类生产、生活关系密切.
铬(Cr)元素与人类生产、生活关系密切.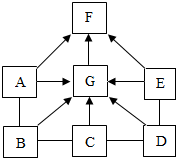 如图中的A~G表示几种初中化学常见的物质,其中A、B是单质,其他均是氧化物;C为红色粉末,B、E为黑色粉末且E中元素质量比为4:1;F是最常用的溶剂.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.
如图中的A~G表示几种初中化学常见的物质,其中A、B是单质,其他均是氧化物;C为红色粉末,B、E为黑色粉末且E中元素质量比为4:1;F是最常用的溶剂.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.