题目内容
8.某同学取氯酸钾和二氧化锰混合物共15.5g,加热至反应完全后剩余固体质量为10.7g.(1)反应生成的氧气的质量为4.8g.
(2)剩余固体中二氧化锰的质量分数为多少?(结果保留小数点后一位)
分析 根据质量守恒定律可知,反应前后固体的质量之差为氧气的质量,然后将氧气的质量代入化学反应方程式来计算氯化钾的质量及二氧化锰的质量,进而计算二氧化锰的质量分数.
解答 解:(1)由质量守恒定律可知,生成氧气的质量为:15.5g-10.7g=4.8g;
(2)设生成氯化钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 4.8g
$\frac{245}{x}$=$\frac{96}{4.8g}$
x=12.25g
所以剩余固体中MnO2的质量为15.5g-12.25g=2.25g,因为催化加在化学反应前后质量不变,所以剩余固体中二氧化锰的质量分数为$\frac{2.25g}{10.7g}$×100%=21.0%.
故答案为:(1)4.8;
(2)21.0%.
点评 根据质量守恒定律,由反应前后固体物质质量差即反应所产生氧气的质量;利用二氧化锰为反应的催化剂,反应前后质量不变,由混合物质量与参加反应的氯酸钾质量差可求得二氧化锰的质量.

练习册系列答案
相关题目
19.下列关于保护金属资源的说法,正确的是( )
| A. | 应及时回收废旧金属 | B. | 应禁止开采金属矿物 | ||
| C. | 应严禁使用金属材料 | D. | 应大力寻找并开采金属矿物 |
16.常温下能与二氧化碳发生化合反应的物质是( )
| A. | 氧气 | B. | 水 | C. | 澄清石灰水 | D. | 木炭 |
3.某大学课题组用石墨烯(石墨烯由石墨制成)制造出了一种超轻物质“碳海绵”,刷新了超轻固体材料的世界纪录,也是目前吸油力最强的材料.下列说法错误的是( )
| A. | “碳海绵”是一种化合物 | |
| B. | “碳海绵”具有较强的吸附作用 | |
| C. | “碳海绵”在一定条件下可与氧化铜发生反应 | |
| D. | “碳海绵”在氧气中完全燃烧的产物是CO2 |
20.下列图示实验操作正确的是( )
| A. |  | B. |  | C. | 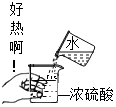 | D. |  |
18.空气中氧气含量测定的再认识.
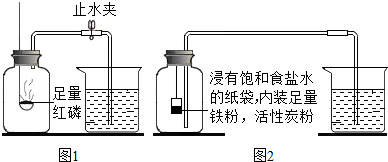
【实验回顾】如图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸入集气瓶中.若装置的气密性良好,操作规范,用量筒测量出进入瓶中水的体积,就能粗略测得空气中氧气的含量.
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
【实验改进】
Ⅰ.根据铁在空气中生锈消耗氧气的原理设计如图2实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
【交流表达】
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气,水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式2Fe+2H2O+O2=2Fe(OH)2.
(2)根据表中数据计算,改进实验后测得空气中氧气的体积分数是20.2%(计算结果精确到0.1%)
(3)从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是:
①铁的缓慢氧化使集气瓶中的氧气消耗更为彻底,使实验结果更准确;②测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确.

【实验回顾】如图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的化学方程式4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸入集气瓶中.若装置的气密性良好,操作规范,用量筒测量出进入瓶中水的体积,就能粗略测得空气中氧气的含量.
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
【实验改进】
Ⅰ.根据铁在空气中生锈消耗氧气的原理设计如图2实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
| 测量项目 | 实验前 | 实验后 | |
| 集气瓶(扣除内容物)和导管的容积 | 烧杯中剩余水的体积 | 烧杯中剩余水的体积 | |
| 体积/mL | 126.0 | 80.0 | 54.5 |
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气,水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式2Fe+2H2O+O2=2Fe(OH)2.
(2)根据表中数据计算,改进实验后测得空气中氧气的体积分数是20.2%(计算结果精确到0.1%)
(3)从实验原理角度分析,改进后的实验结果比前者准确度更高的原因是:
①铁的缓慢氧化使集气瓶中的氧气消耗更为彻底,使实验结果更准确;②测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确.
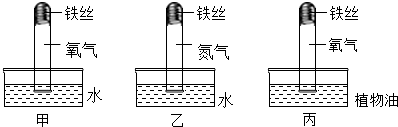
 如图是某胃药标签上的部分内容.某中学化学兴趣小组的同学们测定该药品中碳酸氢钠(NaHCO3)的质量分数,取10片该药品研碎后放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(杂质不溶于水,也不参加反应),共消耗稀盐酸23g.测得反应后烧杯内物质的总质量为25.8g.请计算:
如图是某胃药标签上的部分内容.某中学化学兴趣小组的同学们测定该药品中碳酸氢钠(NaHCO3)的质量分数,取10片该药品研碎后放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(杂质不溶于水,也不参加反应),共消耗稀盐酸23g.测得反应后烧杯内物质的总质量为25.8g.请计算: