题目内容
5. 实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是NaCl、NaOH、Na2CO3、NaHCO3中的一种.小强和小华同学很感兴趣,决定对其成分进行探究:
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是NaCl、NaOH、Na2CO3、NaHCO3中的一种.小强和小华同学很感兴趣,决定对其成分进行探究:提出问题:这瓶试剂可能是什么溶液呢?
交流讨论:根据受损标签的情况判断,这瓶试剂不可能是A
A.酸 B.碱 C.盐
查阅资料:
Ⅰ.Na2CO3和NaHCO3溶液都呈碱性.
Ⅱ.测定室温(20℃)时,四种物质的溶解度的数据如下
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
设计实验并继续探究:
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得PH>7,这瓶试剂不可能是NaCl
.
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加适量的稀盐酸适量的稀盐酸 | 产生大量的气泡 | 该溶液是碳酸钠溶液该溶液是碳酸钠溶液 |
分析 【交流讨论】酸是由氢离子和酸根离子构成,不可能含有钠离子;
【得出结论】根据所给数据可以求出在20℃时各物质的饱和溶液的质量分数,可以做出判断
【设计实验并继续探究】(1)氯化钠溶液呈中性,pH等于7
(2)根据碳酸钠可以和盐酸反应可以设计实验来验证碳酸钠的存在
【拓展与应用】检验碳酸盐的方法较多,例如利用碳酸根可以和钙离子生成沉淀,可以选择钙盐、氢氧化钙等
解答 解:【交流讨论】酸当中不可能含有钠离子,故该溶液不可能是酸,故本题答案为:A;
【得出结论】根据计算可以知道在20℃时饱和碳酸氢钠的质量分数为:$\frac{9.6g}{9.6g+100g}$×100%=8.8%,而题目中标注的溶液的质量分数为10%,所以能够排除碳酸氢钠,故本题答案为:NaHCO3;
【设计实验并继续探究】
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,而氯化钠溶液呈中性,pH等于7所以不可能是氯化钠,故本题答案为:NaCl;
(2)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验:根据碳酸钠可以和盐酸反应可以设计实验来验证碳酸钠的存在,如果产生气泡,则说明是碳酸钠,反之为氢氧化钠,故本题答案为:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 适量的稀盐酸 | 产生大量的气泡 | 该溶液是碳酸钠溶液 相关的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
点评 本题综合利用了物质的组成、物质的溶解性、溶液的酸碱性及物质的变化规律对未知物质进行鉴别,体现运用化学知识分析问题、解决问题的能力.

练习册系列答案
相关题目
15.对有关实验现象的描述不正确的是( )
| A. | 硫在氧气中燃烧发出明亮蓝紫色火焰 | |
| B. | 浓盐酸敞口放置在空气中瓶口猫“白雾” | |
| C. | 铁丝在氧气中燃烧生成白色固体四氧化三铁 | |
| D. | 红磷在氧气中燃烧产生白烟 |
16.下列物质鉴别的实验方法错误的是( )
| 鉴别物质 | 实验方法 |
| A过氧化氢和蒸馏水 | 分别加入MnO2,看是否有气泡 |
| B镁和锌 | 分别加入稀盐酸,看是否有气泡 |
| C二氧化碳、氧气和空气 | 将燃着的木条分别伸入瓶中,观察现象 |
| D活性炭和氧化铜 | 分别投入盛有红棕色二氧化氮气体的集气瓶中,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
10.某同学为了确认某种溶液是否可能为稀盐酸,他取少量这种溶液进行如下实验,其中错误的是( )
| A. | 在取出的溶液中滴入几滴石蕊溶液 | B. | 在取出的溶液中加入石灰石 | ||
| C. | 尝一尝取出溶液是否有酸味 | D. | 在取出的溶液中加入锌粒 |
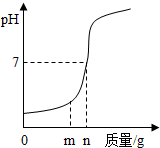 (1)用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.熟石灰与盐酸反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H20;当加入熟石灰m g时,溶液中的溶质为CaCl2和HCl.若改用n g氢氧化钠与相同量盐酸反应,所得溶液的pH<7(填“>”“<”或“=”).
(1)用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示.熟石灰与盐酸反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H20;当加入熟石灰m g时,溶液中的溶质为CaCl2和HCl.若改用n g氢氧化钠与相同量盐酸反应,所得溶液的pH<7(填“>”“<”或“=”).
