题目内容
下列实验设计方案或判断合理的是
A. 鉴别氢氧化镁和氯化钠固体:取样,分别滴加足量的稀盐酸
B. 向含有某种杂质的氯化钡溶液中通入二氧化碳:若出现白色沉淀,则杂质一定含氢氧根离子
C. 分离氯化钡和氯化钠溶液:滴加适量的碳酸钠溶液,过滤
D. 检验碳酸钠溶液中是否含有氢氧化钠:取样,先滴加足量的氢氧化钙溶液,再滴加酚酞
B 【解析】A、氢氧化镁可以与稀盐酸反应,固体溶解,氯化钠与稀盐酸不反应,但是可以溶解在稀盐酸的溶解中,固体溶解,故不能鉴别,错误; B、向含有某种杂质的氯化钡溶液中通入二氧化碳:若不含其它杂质,则不能生成白色的碳酸钡沉淀,因为若该反应能进行,生成的盐酸又会使白色沉淀消失,若出现白色沉淀,一定是杂质中含有氢氧根消耗了盐酸,反应才能出现白色沉淀,正确; C、分离氯化钡和氯化钠溶液:...
练习册系列答案
相关题目
小红学碱的性质时做了如图两个实验,并把两个实验的滤液都倒入了一个烧杯中,结果烧杯中产生了少量气泡,最终还有白色沉淀生成。回答下列问题:
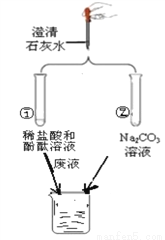
(1)实验①中酚酞溶液的作用___________________。
(2)实验②中滤液的溶质除有氢氧化钠外,还有________________(填化学式)。
(3)烧杯中产生白色沉淀物的化学方程式 ____________。
(4)小红对烧杯中的溶质的成分进行探究:小红认为除有NaCl外,还可能含有:
猜想1:还可能含有CaCl2
猜想2: 还可能含有___________,为了验证猜想1提出方案如下:
实验操作 | 实验现象 | 实验结论 |
取烧杯中的少量滤液于试管中,加入Na2CO3溶液 | _____________________ | 猜想1正确 |
除去下列物质中的杂质(括号内为杂质),所用试剂或方法不正确的是
选项 | 物质(杂质) | 除杂质所用试剂或方法 |
A | FeSO4溶液( CuSO4溶液 ) | 加入足量铁粉,过滤 |
B | NaOH溶液 (Na2CO3溶液) | 加入适量Ca(OH)2溶液,结晶 |
C | H2气体( HCl气体) | 依次通过碳酸钠溶液和浓硫酸 |
D | CuO粉末(C粉) | 在空气中充分灼烧 |
A. A B. B C. C D. D
BC 【解析】A、足量铁粉能与CuSO4溶液反应生成硫酸亚铁溶液和铜,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,正确;B、碳酸钠能与适量的氢氧化钙溶液反应生成碳酸钙沉淀和氢氧化钠,结晶得到的固体中含有碳酸钙,能除去杂质且引入新的杂质,不符合除杂原则,错误;C、碳酸钠溶液与盐酸反应有二氧化碳气体生成,能除去杂质且引入新的杂质,不符合除杂原则,错误;D、C粉在空气中灼烧生成二氧化碳气体...
