题目内容
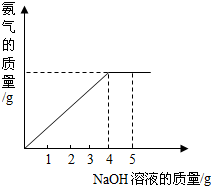 硝酸铵是农业生产中常用的化学肥料.为测定某含有少量NaNO3的硝酸铵样品中NH4NO3的纯度,取2.0g该硝酸铵样品于容器中,滴入5.0g20%的NaOH溶液.发生如下反应:NH4NO3+NaOH=NaNO3+NH3↑+H2O.反应过程中放出的氨气质量及加入的NaOH溶液的质量的关系如图所示:完成有关计算:
硝酸铵是农业生产中常用的化学肥料.为测定某含有少量NaNO3的硝酸铵样品中NH4NO3的纯度,取2.0g该硝酸铵样品于容器中,滴入5.0g20%的NaOH溶液.发生如下反应:NH4NO3+NaOH=NaNO3+NH3↑+H2O.反应过程中放出的氨气质量及加入的NaOH溶液的质量的关系如图所示:完成有关计算:(1)NH4NO3中氮元素的质量分数为
(2)现有20.0g5%的NaOH溶液,欲配制20%的NaOH溶液,需固体NaOH
(3)样品中硝酸铵的纯度是多少?
(4)恰好完全反应时所得溶液中NaNO3的质量分数(保留一位小数)?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算,元素的质量分数计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)利用硝酸铵的化学式即可求出氮元素的质量分数.
(2)依据溶液稀释前后溶质的质量不会变化分析解答;
(3)从图中可看出氢氧化钠溶液滴加到4克时硝酸铵恰好完全反应,根据参加反应的氢氧化钠的质量求出硝酸铵的质量,再求出样品中硝酸铵的质量分数.
(4)根据参加反应的氢氧化钠的质量求出生成的硝酸钠的质量,用生成的硝酸钠的质量+原有的硝酸钠的质量为所得溶液中硝酸钠的质量;用样品的质量+所加氢氧化钠溶液的质量-氨气的质量(氨气的质量可根据氢氧化钠的质量求出)为所得溶液的质量;即可求出所得溶液中硝酸钠的质量分数.
(2)依据溶液稀释前后溶质的质量不会变化分析解答;
(3)从图中可看出氢氧化钠溶液滴加到4克时硝酸铵恰好完全反应,根据参加反应的氢氧化钠的质量求出硝酸铵的质量,再求出样品中硝酸铵的质量分数.
(4)根据参加反应的氢氧化钠的质量求出生成的硝酸钠的质量,用生成的硝酸钠的质量+原有的硝酸钠的质量为所得溶液中硝酸钠的质量;用样品的质量+所加氢氧化钠溶液的质量-氨气的质量(氨气的质量可根据氢氧化钠的质量求出)为所得溶液的质量;即可求出所得溶液中硝酸钠的质量分数.
解答:解:(1)在NH4NO3中氮元素的质量分数为
×100%=35%
(2)设需要氢氧化钠固体的质量是m
m+20g×5%=(20g+m)×20%
m=3.75g
(3)设2.0g样品中含NH4NO3的质量为x,反应生成NaNO3的质量为y,反应生成的NH3的质量为z,
NH4NO3+NaOH═NaNO3+NH3↑+H2O
80 40 85 17
x 4g×20% y z
=
=
=
x=1.6g y=1.7g z=0.34g
样品中硝酸铵的质量分数=
×100%=80.00%
(4)所得溶液中硝酸钠的质量=2.00g-1.60g+1.70g=2.1g
所得溶液的质量=2.00g+5.0g-0.34g=6.66g
所得溶液中硝酸钠的质量分数=
×100%=31.5%
故答案为:(1)35%;(2)3.75;(3)样品中硝酸铵的纯度是80%;(3)答:所得溶液中硝酸钠的质量分数为31.5%
| 2×14 |
| 2×14+4+16×3 |
(2)设需要氢氧化钠固体的质量是m
m+20g×5%=(20g+m)×20%
m=3.75g
(3)设2.0g样品中含NH4NO3的质量为x,反应生成NaNO3的质量为y,反应生成的NH3的质量为z,
NH4NO3+NaOH═NaNO3+NH3↑+H2O
80 40 85 17
x 4g×20% y z
| 80 |
| x |
| 40 |
| 4g×20% |
| 85 |
| y |
| 17 |
| z |
x=1.6g y=1.7g z=0.34g
样品中硝酸铵的质量分数=
| 1.6g |
| 2g |
(4)所得溶液中硝酸钠的质量=2.00g-1.60g+1.70g=2.1g
所得溶液的质量=2.00g+5.0g-0.34g=6.66g
所得溶液中硝酸钠的质量分数=
| 2.1g |
| 6.66g |
故答案为:(1)35%;(2)3.75;(3)样品中硝酸铵的纯度是80%;(3)答:所得溶液中硝酸钠的质量分数为31.5%
点评:本题主要考查学生运用化学方程式和质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
下列反应中,属于化合反应的是( )
A、氢气+氧气
| ||
B、石蜡+氧气
| ||
C、氧化汞
| ||
D、氧气
|
下列说法正确的是( )
| A、溶液一定是均一的、稳定的混合物 |
| B、原子中质子数一定等于中子数 |
| C、能使石蕊试液变蓝的溶液一定是碱溶液 |
| D、由同种元素组成的物质一定是单质 |
下列反应用作鉴定CO2气体的是( )
| A、CO2+H2O=H2CO3 |
| B、H2CO3=CO2↑+H2O |
| C、CO2+C═2CO |
| D、CO2+Ca(OH)2=H2O+CaCO3↓ |