��Ŀ����
��7�֣���Һ��Ӧ�÷dz��㷺��
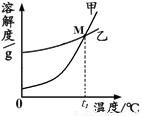
��1��K2CO3��KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȼ����ܽ���������¡�
|
�¶�/�� |
20 |
30 |
50 |
60 |
80 |
|
|
�ܽ��/g |
K2CO3 |
110 |
114 |
121 |
126 |
139 |
|
KNO3 |
31.6 |
45.8 |
85.5 |
110 |
169 |
��ͼ���ܱ�ʾKNO3�ܽ�����ߵ��� ����ס����ҡ�����
��������M������ ��
��20��ʱ��K2CO3������Һ���������ܼ���������Ϊ ���������������ȱ�ʾ����
��30��ʱ����114 g K2CO3�����м���100 gˮ������ܽ��������40�棬����Һ�����ʵ��������� ����������С�����䡱����
��2��ijKNO3��Ʒ�к�������K2CO3�����ᴿ�������£�
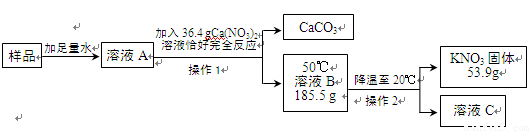
С���ϣ�K2CO3 + Ca(NO3)2 = CaCO3��+ 2KNO3
�ٲ���2�������� ��
����ҺB����ҺC�����ڱ�����Һ���� ������ţ���
����Ʒ�м�Ԫ�ص�����Ϊ g�����������������
��1���ټ� �� t1��ʱ��KNO3��K2CO3���ܽ����� ��11��10 �ܲ���
��2���ٹ��� ��B C ��33
��������
�����������1�������������ݿ�֪������ص��ܽ�����¶�Ӱ��ϴ�ͼ���ܱ�ʾKNO3�ܽ�����ߵ��Ǽף�
��������M��ĺ�����t1��ʱ��KNO3��K2CO3���ܽ����ȣ�
��20��ʱ��̼��ص��ܽ����110g���ʴ�ʱK2CO3������Һ���������ܼ���������Ϊ110��100=11��10��
��30��ʱ����114 g K2CO3�����м���100 gˮ������ܽ��������40�棬����Һ�����ʺ��ܼ����������䣬�ʸ���Һ�����ʵ������������䡣
��2���ٲ���2�ǽ�������Һ����룬�������ǹ��ˣ�
��50��ʱ������ص��ܽ����85.5g����ҺC�ǽ��º���������ı�����Һ������ҺB����ҺC�����ڱ�����Һ��
��50��ʱ������ص��ܽ����85.5g��50��ʱ��185.5g����ر�����Һ�к��������85.5g������Ʒ�м�Ԫ�ص�����Ϊ85.5��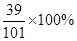 =33g
=33g
���㣺�ܽ�ȣ��ܽ�����ߣ���������������
�������ܽ������һ���¶��£�ij������100gˮ�У��ܽ�ﵽ����״̬ʱ�ܽ������������
������������=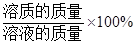 ��
��


 ��������������Һ��Ӧ�÷dz��㷺��K2CO3��KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȼ����ܽ��������ͼ��
��������������Һ��Ӧ�÷dz��㷺��K2CO3��KNO3�ڲ�ͬ�¶�ʱ���ܽ�ȼ����ܽ��������ͼ��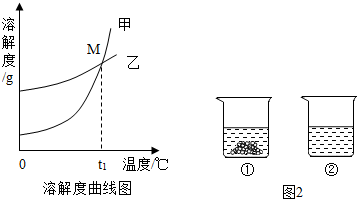

 ��2013?�����ж�ģ����Һ��Ӧ�÷dz��㷺��
��2013?�����ж�ģ����Һ��Ӧ�÷dz��㷺��